题目内容
下列叙述不正确的是( )
| A、金属腐蚀的本质是金属原子失去电子而被氧化 |
| B、将地下钢管与直流电源的正极相连,用来保护钢管 |
| C、电解饱和食盐水制氢氧化钠,可以用铁做阴极 |
| D、氢氧燃料电池中,氢气在负极发生氧化反应 |
考点:金属的电化学腐蚀与防护,原电池和电解池的工作原理
专题:电化学专题
分析:A、金属原子失去电子被氧化;
B、钢管与直流电源的正极相连,阳极金属易被腐蚀;
C、在阴极上是发生得电子的还原反应;
D、燃料电池中,燃料在负极发生氧化反应.
B、钢管与直流电源的正极相连,阳极金属易被腐蚀;
C、在阴极上是发生得电子的还原反应;
D、燃料电池中,燃料在负极发生氧化反应.
解答:
解:A、金属腐蚀的本质是金属原子在负极上失去电子而被氧化的过程,故A正确;
B、将地下钢管与电源负极相连,作电解池的阴极被保护,能防止钢铁锈蚀,故B错误;
C、电解饱和食盐水制氢氧化钠,在阴极区会产生氢氧化钠,金属铁必须做阴极,不能做阳极,故C正确;
D、氢氧燃料电池中,在负极上是燃料发生氧化反应的过程,故D正确.
故选B.
B、将地下钢管与电源负极相连,作电解池的阴极被保护,能防止钢铁锈蚀,故B错误;
C、电解饱和食盐水制氢氧化钠,在阴极区会产生氢氧化钠,金属铁必须做阴极,不能做阳极,故C正确;
D、氢氧燃料电池中,在负极上是燃料发生氧化反应的过程,故D正确.
故选B.
点评:本题考查学生金属的腐蚀和防护知识以及燃料电池的工作原理知识,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质中不能有两种单质直接反应生成的是( )
| A、Na2O |
| B、Na2O2 |
| C、Fe3O4 |
| D、FeCl2 |
下列化学反应的有机产物中,存在同分异构体的是( )
| A、(CH3)2CHCH2Br在碱性溶液中水解 |
| B、苯在催化剂FeCl3作用下与Cl2反应 |
C、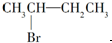 与NaOH的醇溶液共热反应 与NaOH的醇溶液共热反应 |
D、 在催化剂存在下与H2完全加成 在催化剂存在下与H2完全加成 |
若在加入铝粉能放出氢气的溶液中分别加入下列各组离子,可能共存的是( )
| A、Ag+ K+ Ba2+ I- |
| B、[Al(OH)4]- S2- HCO3-Na+ |
| C、NH4+Fe3+Cl-SO42- |
| D、Fe2+Cu2+Mg2+NO3- |
关于醋酸的下列说法不正确的是( )
| A、既能与有机物反应又能与无机物反应 |
| B、既能发生复分解反应又能发生水解反应 |
| C、既能发生置换反应又能发生酯化反应 |
| D、既能发生取代反应又能发生氧化还原反应 |
设NA为阿伏加德罗常数的数值,下列说法不正确的是( )
| A、PH=1的硫酸溶液1 L,则该硫酸溶液中氢离子数目为0.1NA |
| B、常温下,14g C2H4和C3H6的混合气体中含有2NA个碳原子 |
| C、2.3 g Na和足量的O2完全反应,在常温和燃烧时,转移电子数均为0.1NA |
| D、1mol甲烷中含有C-H键的数目为4NA |
设NA表示阿伏加德罗常数,下列说法正确的是( )
| A、含NA个Na+的Na2O2与1L水完全反应后所得溶液中Na+的物质的量浓度为1mol/L | ||
B、H2O通过Na2O2使其增重6 g时,反应中转移的电子数为
| ||
| C、6.2g氧化钠和7.8g过氧化钠的混合物中含有的离子总数为0.6NA | ||
| D、常温下,286 g Na2CO3?10H2O晶体中含有的CO32-小于NA个 |