题目内容
将pH=3的硫酸溶液和pH=10的氢氧化钠溶液相混合,若要使混合后溶液的pH=7,则硫酸溶液和氢氧化溶液的体积比约为( )
| A、1:2 | B、1:9 |
| C、1:10 | D、1:20 |
考点:pH的简单计算
专题:电离平衡与溶液的pH专题
分析:pH=3的H2SO4溶液中c(H+)=1×10-3mol/L,pH=10的NaOH溶液,根据Kw=c(OH-)×c(H+),计算出氢氧根离子的浓度;
pH=3的H2SO4溶液和pH=10的NaOH溶液混合,混合液的pH=7,则说明酸碱恰好完全反应,应满足n(OH-)=n(H+),设出硫酸和氢氧化钠溶液体积,然后列式计算.
pH=3的H2SO4溶液和pH=10的NaOH溶液混合,混合液的pH=7,则说明酸碱恰好完全反应,应满足n(OH-)=n(H+),设出硫酸和氢氧化钠溶液体积,然后列式计算.
解答:
解:设pH=3的H2SO4溶液xL、pH=10的NaOH溶液yL混合,
pH=3的H2SO4溶液,c(H+)=1×10-3mol/L,
pH=10的NaOH溶液,根据Kw=c(OH-)×c(H+),c(OH-)=
mol/L=1×10-4mol/L,
混合液的pH=7,所得混合液为中性,酸碱恰好完全反应,n(H+)=n(OH-),
则:1×10-3mol/L×xL=1×10-4mol/L×yL,
解得x:y=1:10,
故选C.
pH=3的H2SO4溶液,c(H+)=1×10-3mol/L,
pH=10的NaOH溶液,根据Kw=c(OH-)×c(H+),c(OH-)=
| 1×10-14 |
| 1×10-10 |
混合液的pH=7,所得混合液为中性,酸碱恰好完全反应,n(H+)=n(OH-),
则:1×10-3mol/L×xL=1×10-4mol/L×yL,
解得x:y=1:10,
故选C.
点评:本题考查了溶液酸碱性与溶液pH的计算,题目难度中等,注意掌握溶液酸碱性与溶液pH的关系,明确溶液中氢离子、氢氧根离子浓度与溶液pH的关系为解答本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
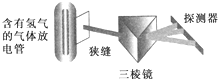 在实验室中用下列的装置可以得到氢原子光谱,实验证明该光谱为线状光谱,该光谱的发现在原子结构的认识过程中,有极为重要的意义,根据它产生了( )
在实验室中用下列的装置可以得到氢原子光谱,实验证明该光谱为线状光谱,该光谱的发现在原子结构的认识过程中,有极为重要的意义,根据它产生了( )| A、卢瑟福核式原子模型 |
| B、汤姆逊“葡萄干布丁”模型 |
| C、玻尔核外电子分层排布模型 |
| D、原子结构的量子力学模型 |
10mL 0.05mol/L含有R2O72-离子的浓溶液恰好能将60mL 0.05mol/L的Fe2+溶液完全氧化,则元素R在还原产物中的化合价为( )
| A、+1价 | B、+2价 |
| C、+3价 | D、+6价 |
液氨是富氢物质,是氢能的理想载体,利用N2+3H2
2NH3实现储氢和输氢.下列说法不正确的是 ( )
| 催化剂 |
| A、NH3分子中N原子采用sp2杂化 |
| B、相同压强时,NH3沸点比PH3高 |
| C、[Cu(NH3)4]2+离子中,N原子是配位原子 |
D、CN-的电子式为: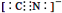 |
下列说法中正确的是( )
| A、复分解反应一定是氧化还原反应 |
| B、化合反应一定不是氧化还原反应 |
| C、分解反应一定是氧化还原反应 |
| D、置换反应一定是氧化还原反应 |
“对氨基苯甲酸正丁酯”是防晒霜中能吸收紫外线的防晒剂.下列关于“对氨基苯甲酸正丁酯”的说法正确的是( )
| A、它的分子式是C11H15NO2 |
| B、从有机物分类看,它可属于“氨基酸类”、“酯类”、“芳香烃类” |
| C、它能与盐酸反应,也能与苛性钠溶液反应 |
| D、甲酸丁酯基(-COOC4H9)有三种不同结构 |
下列离子方程式书写正确的是( )
| A、钠投入水中:Na+H2O=Na++OH-+H2↑ |
| B、将铝投入足量的氨水:2Al+2OH-+2H2O=2AlO2-+3H2↑ |
| C、NaHCO3中加入盐酸:HCO3-+H+=CO2↑+H2O |
| D、钠与CuSO4溶液反应:2Na+Cu2+=2Na++Cu |