题目内容
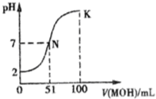 常温下,向l00mL 0.01mol/L HA的溶液中逐滴加入0.02mol/L MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中不正确的是( )
常温下,向l00mL 0.01mol/L HA的溶液中逐滴加入0.02mol/L MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中不正确的是( )| A、HA为一元强酸 | ||
| B、N点水的电离程度小于K点水的电离程度 | ||
C、随着MOH溶液的滴加,比值
| ||
| D、若K点对应的溶液的PH=10,则有c(MOH)+c(OH-)-c(H+)=0.005mol/L |
考点:酸碱混合时的定性判断及有关ph的计算,pH的简单计算
专题:电离平衡与溶液的pH专题
分析:A.根据0.01mol/L的HA溶液的pH=2可知,HA在溶液中完全电离,则HA为强电解质;
B.N点为中性溶液,而K点溶液显示碱性,氢氧根离子抑制了水电离电离;
C.
为MOH的电离平衡常数,电离平衡常数只受温度的影响;
D.根据物料守恒、电荷守恒判断溶液中c(MOH)+c(OH-)-c(H+)结果.
B.N点为中性溶液,而K点溶液显示碱性,氢氧根离子抑制了水电离电离;
C.
| c(M+)?c(OH-) |
| c(MOH) |
D.根据物料守恒、电荷守恒判断溶液中c(MOH)+c(OH-)-c(H+)结果.
解答:
解:A.根据图象可知,加入氢氧化钠溶液前,0.01mol?L-1HA溶液的pH=2,说明HA在溶液中完全电离,则HA是强酸,故A正确;
B.由图象可知,N点溶液呈中性,水电离的氢离子为10-7mol/l,K点溶液呈碱性,MOH电离的氢氧根离子抑制了水电离,水电离的氢离子小于10-7mol/l,所以N点水的电离程度大于K点水的电离程度,故B错误;
C.比值
为MOH的电离平衡常数,只受温度的影响,温度不变,则其值不变,故C正确;
D.在K点时混合溶液体积是碱溶液的2倍,根据物料守恒结合溶液体积变化知,c(MOH)+c(M+)=0.01mol?L-1,根据电荷守恒得c(M+)+c(H+)=c(OH-)+c(A-),c(MOH)+c(OH-)-c(H+)=c(M+)-c(A-)+c(MOH)=0.01mol?L-1-0.005mol?L-1=0.005mol?L-1,故D正确;
故选B.
B.由图象可知,N点溶液呈中性,水电离的氢离子为10-7mol/l,K点溶液呈碱性,MOH电离的氢氧根离子抑制了水电离,水电离的氢离子小于10-7mol/l,所以N点水的电离程度大于K点水的电离程度,故B错误;
C.比值
| c(M+)?c(OH-) |
| c(MOH) |
D.在K点时混合溶液体积是碱溶液的2倍,根据物料守恒结合溶液体积变化知,c(MOH)+c(M+)=0.01mol?L-1,根据电荷守恒得c(M+)+c(H+)=c(OH-)+c(A-),c(MOH)+c(OH-)-c(H+)=c(M+)-c(A-)+c(MOH)=0.01mol?L-1-0.005mol?L-1=0.005mol?L-1,故D正确;
故选B.
点评:本题考查了酸碱混合时的定性判断、弱电解质电离及其影响因素,题目难度中等,注意掌握溶液酸碱性与溶液pH的关系,选项D为易错点,可以根据物料守恒和电荷守恒来分析解答.

练习册系列答案
相关题目
下列与有机物结构、性质相关的叙述中,正确的是( )
| A、淀粉、纤维素都属于天然高分子化合物,二者分子式相同,互为同分异构体 |
| B、粮食酿造的酒一定温度下密封存放时间越长香味越浓,是因为有酯生成 |
| C、鸡蛋清中加入CuSO4溶液会产生盐析现象,析出的蛋白质可再溶于水 |
| D、石油化工中的分馏、裂化、裂解都是通过化学反应来获得轻质油、气体烯烃 |
设NA为阿伏加德罗常数,下列叙述中正确的是( )
| A、80g硝酸铵含有氮原子数为2NA |
| B、1L 1mol/L的盐酸溶液中,所含氯化氢分子数为NA |
| C、标准状况下,11.2L SO3所含分子数为0.5 NA |
| D、0.1mol FeCl3加入沸水中,全部制得Fe(OH)3胶体,胶体粒子数为0.1NA |
下列说法正确的是( )
| A、糖类、油脂、蛋白质都能发生水解反应 |
| B、油脂有油和脂肪之分,都属于酯类 |
| C、糖类、油脂、蛋白质都是由C、H、O三种元素组成的 |
| D、糖类、油脂、蛋白质都是高分子化合物 |
如图所示,其中甲池的总反应式为:2CH3OH+3O2+4KOH=2K2CO3+6H2O下列说法正确的是( )
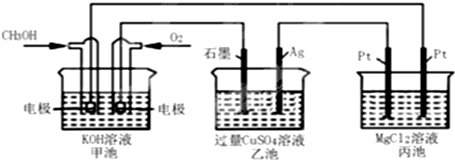

| A、甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置 |
| B、甲池通入CH3OH的电极反应为CH3OH-6e-+2H2O=CO32-+8H+ |
| C、甲池中消耗280mL(标准状况下)O2,此时丙池中理论上最多产生1.45g固体 |
| D、反应一段时间后,向乙池中加入一定量Cu(OH)2固体,能使CuSO4溶液恢复到原浓度 |
某学生用托盘天平称量食盐时,他将食盐放在右盘,砝码放在左盘,称得食盐的质量为15.5g(1g以下使用游码添加质量).该学生所称量的食盐的实际质量为( )
| A、14.5g |
| B、15.5g |
| C、16.0g |
| D、15.0g |
下列关于甲烷与氯气发生取代反应所得生成物的说法正确的是( )
| A、都是有机物 |
| B、都不溶于水 |
| C、有一种气态物质,其余都是液体 |
| D、有一种是无机物其余都是有机物 |