下列离子方程式书写正确的是( )
| A、NaHSO4溶液与Ba(OH)2溶液混合后溶液呈中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O | ||||
| B、将标准状况下112 mL氯气通入10 mL 1 mol?L-1的溴化亚铁溶液中:2Fe2++4Br-+3Cl2=2Fe3++6Cl-+2Br2 | ||||
C、用惰性电极电解饱和MgCl2溶液:2Cl-+2H2O
| ||||
| D、向澄清石灰水中加入过量的碳酸氢钠溶液:Ca2++OH-+HCO3-=CaCO3↓+H2O |
电解质在工农业生产和各种生命活动中都起着重要作用,下列有关电解质的叙述正确的是( )
| A、强电解质溶液比弱电解质溶液的导电能力强 |
| B、电解质一定是化合物 |
| C、SO3 溶于水形成的溶液能导电,所以SO3 是电解质 |
| D、NaCl固体不导电,所以NaCl不是电解质 |
在相同温度下,等体积等物质的量浓度的4种稀溶液:①Na2SO4、②H2S、③NaHSO3、④Na2S中所含带电微粒数由多到少的顺序是( )
| A、①=④>③=② |
| B、④=①>③>② |
| C、①>④>③>② |
| D、④>①>③>② |
下列各组离子能在指定环境中大量共存的是( )
A、c(HCO
| ||||||
B、室温下,由水电离出的c(H+)=1×10-12 mol?L-1的溶液中:Fe2+、ClO-、Na+、SO
| ||||||
C、无色透明溶液中:SO
| ||||||
D、使红色石蕊试纸变蓝的溶液中:SO
|
下列物质中既有离子键,又有共价键的是( )
| A、H2O |
| B、CaCl2 |
| C、NH4NO3 |
| D、Cl2 |
下列化学反应所对应的离子方程式正确的是( )
| A、金属铝和过量的氢氧化钠溶液反应:2OH-+Al═AlO2-+H2↑ |
| B、氯化铁溶液中加入铁粉:2Fe3++Fe═3Fe2+ |
| C、稀硫酸与氢氧化钡溶液反应:H++OH-═H2O |
| D、向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- |
等体积等物质的量浓度的硫酸,氢氧化钠溶液分别放在甲、乙两烧杯中,各加等质量的铝,生成氢气的体积比为4:5,则甲、乙两烧杯中的反应情况可能分别是( )
| A、甲、乙中都是铝过量 |
| B、甲中铝过量,乙中碱过量 |
| C、甲中酸过量,乙中铝过量 |
| D、甲中酸过量,乙中碱过量 |
下列各有机物的分类或命名正确的是( )
A、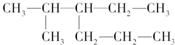 2甲基3丙基戊烷 2甲基3丙基戊烷 |
B、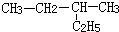 2-乙基丁烷 2-乙基丁烷 |
C、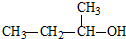 2-甲基-1-丙醇 2-甲基-1-丙醇 |
D、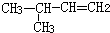 3-甲基-1-丁烯 3-甲基-1-丁烯 |
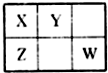 X、Y、Z、W均为短周期元素,它们在周期表中的位置如图所示.若X原子的最外层电子数比其次外层电子数多3个,下列说法正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中的位置如图所示.若X原子的最外层电子数比其次外层电子数多3个,下列说法正确的是( )| A、Y位于第二周期第ⅣA族 |
| B、非金属性:Y>Z>X |
| C、原子半径:Z>Y>X |
| D、X、W的氢化物相遇会产生白烟 |
已知:2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol;
Na2O2(s)+CO2(g)=Na2CO3(s)+
O2(g)△H=-226kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )
Na2O2(s)+CO2(g)=Na2CO3(s)+
| 1 |
| 2 |
根据以上热化学方程式判断,下列说法正确的是( )
| A、CO的燃烧热为283 kJ |
B、 如图可表示由CO生成CO2的反应过程和能量关系 |
| C、2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g)△H>-452 kJ/mol |
| D、CO2(g)与Na2O2(s)反应放出452kJ热量时,电子转移数为1.204×1024个 |