题目内容
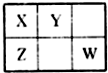 X、Y、Z、W均为短周期元素,它们在周期表中的位置如图所示.若X原子的最外层电子数比其次外层电子数多3个,下列说法正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中的位置如图所示.若X原子的最外层电子数比其次外层电子数多3个,下列说法正确的是( )| A、Y位于第二周期第ⅣA族 |
| B、非金属性:Y>Z>X |
| C、原子半径:Z>Y>X |
| D、X、W的氢化物相遇会产生白烟 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:X、Y、Z、W均为短周期元素,由元素在周期表中的位置,可知X、Y处于第二周期,Z、W处于第三周期,若X原子的最外层电子数比其次外层电子数多3个,则其最外层电子数为5,故X为N元素,可推知Y为O元素,Z为P元素,W为Cl,据此解答.
解答:
解:X、Y、Z、W均为短周期元素,由元素在周期表中的位置,可知X、Y处于第二周期,Z、W处于第三周期,若X原子的最外层电子数比其次外层电子数多3个,则其最外层电子数为5,故X为N元素,可推知Y为O元素,Z为P元素,W为Cl,
A.Y为氧元素,位于第二周期第ⅥA族,故A错误;
B.同周期自左而右元素非金属性增强,同主族自上而下元素非金属性减弱,故非金属性O>N>P,故B错误;
C.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径P>N>O,故C错误;
D.X、W的氢化物分别为氨气、HCl,二者相遇反应生成氯化铵固体颗粒,会产生白烟,故D正确,
故选D.
A.Y为氧元素,位于第二周期第ⅥA族,故A错误;
B.同周期自左而右元素非金属性增强,同主族自上而下元素非金属性减弱,故非金属性O>N>P,故B错误;
C.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径P>N>O,故C错误;
D.X、W的氢化物分别为氨气、HCl,二者相遇反应生成氯化铵固体颗粒,会产生白烟,故D正确,
故选D.
点评:本题考查结构性质位置关系应用,推断元素是解题关键,注意对元素周期律的理解掌握,难度不大.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
下列分子或离子中,能提供孤对电子与某些金属离子形成配位键的是( )
①H2O ②NH3 ③Cl- ④CN- ⑤CO.
①H2O ②NH3 ③Cl- ④CN- ⑤CO.
| A、①② | B、①②③ |
| C、①②④ | D、①②③④⑤ |
2012年白酒行业塑化剂风波成为人们关注的焦点,塑化剂的其中一种邻苯二甲酸二丁酯(DBP)的结构如图所示,可由邻苯二甲酸(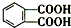 )与正丁醇发生酯化反应制得,下列有关说法不正确的是( )
)与正丁醇发生酯化反应制得,下列有关说法不正确的是( )
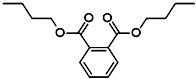
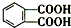 )与正丁醇发生酯化反应制得,下列有关说法不正确的是( )
)与正丁醇发生酯化反应制得,下列有关说法不正确的是( )
| A、邻苯二甲酸二丁酯(DBP)分子式为:C16H22O4 |
| B、邻苯二甲酸二丁酯(DBP)苯环上的一氯代物有2种 |
| C、邻苯二甲酸二丁酯(DBP)属于苯的同系物 |
| D、丁醇有4种不同结构,正丁醇是其中的一种,分子式为C4H10O |
2009年卫生部印发了《饮水型地方性砷中毒监测方案(试行)的通知》.已知在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:3SnCl2+12Cl-+2H3AsO3+6H+═2As+3SnCl62-+6M,关于该反应的说法中正确的组合是( )
①SnCl2是还原剂
②还原性:Cl->As
③每生成7.5gAs,还原剂失去的电子为0.3mol
④M为H2O
⑤SnCl62-是氧化产物.
①SnCl2是还原剂
②还原性:Cl->As
③每生成7.5gAs,还原剂失去的电子为0.3mol
④M为H2O
⑤SnCl62-是氧化产物.
| A、①③④⑤ | B、①②④⑤ |
| C、①②③④ | D、①③ |
已知N2O4(g)?2NO2(g)△H>0,现将1mol N2O4充入一恒压密闭容器中,如图示意图正确且能说明反应达到平衡状态的是( )
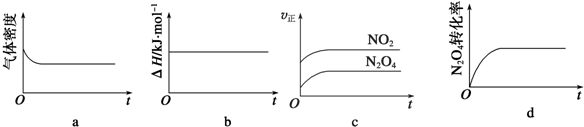

| A、ab | B、bc | C、ac | D、ad |
下列各组离子能在指定环境中大量共存的是( )
A、c(HCO
| ||||||
B、室温下,由水电离出的c(H+)=1×10-12 mol?L-1的溶液中:Fe2+、ClO-、Na+、SO
| ||||||
C、无色透明溶液中:SO
| ||||||
D、使红色石蕊试纸变蓝的溶液中:SO
|
在一定条件下,测得2CO2?2CO+O2(反应从CO2开始)平衡体系的平均相对分子质量为M,在此条件下,CO2的分解率为( )
A、
| ||
B、
| ||
C、
| ||
D、
|