用如图实验装置和方法进行相应实验,能达到实验目的是( )
A、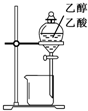 分离乙醇与乙酸 |
B、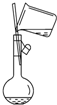 向容量瓶中转移液体 |
C、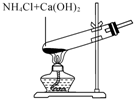 制备少量氨气 |
D、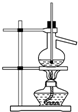 分馏石油 |
室温下,用含 0.2mol NaOH的溶液恰好吸收0.2mol NO2后得1L溶液,反应的化学方程式为:2NO2+2NaOH→NaNO3+NaNO2+H2O.对反应后的溶液,下列说法正确的是(已知:Ka(HNO2)=7.1×10-4、Ka(CH3COOH)=1.7×10-5)( )
| A、n(NO2-)+n(OH-)-n(H+)=0.1 mol |
| B、若通入0.01 mol HCl气体,溶液pH大于2(忽略溶液体积的变化) |
| C、若加入少量CH3COONa固体,溶液的碱性会减弱 |
| D、此时溶液的pH大于0.1 mol/L的CH3COONa溶液 |
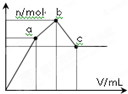 向100mL 0.1mol?L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1mol?L-1 Ba(OH)2溶液.随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示.则下列说法中正确的是( )
向100mL 0.1mol?L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1mol?L-1 Ba(OH)2溶液.随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示.则下列说法中正确的是( )| A、a点的溶液呈中性 |
| B、b点发生反应的离子方程式是:Al3++2SO42-+2Ba2++3OH-═Al(OH)3↓+2BaSO4↓ |
| C、c点加入Ba(OH)2溶液的体积为200mL |
| D、c点溶液呈碱性 |
现有BaCl2和NaCl的混合溶液a L,分成两份,一份滴加稀硫酸,除去Ba2+;另一份滴加硝酸银溶液,除去Cl-,反应中消耗稀硫酸x mol,硝酸银y mol,则原溶液中的Na+的物质的量浓度为 .
500mL含有0.40mol碳酸钠的溶液和某浓度的400mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是( )
| A、1.2mol/L |
| B、2 mol/L |
| C、0.2 mol/L |
| D、0.4mol/L |
已知:将一定量Cl2通入KOH溶液,可能生成KCl、KClO、KClO3,且
的值与温度高低有关.当n(KOH)=6a mol时,下列有关说法错误的是( )
| c(Cl-) |
| c(ClO-) |
A、若某温度下,反应后
| ||||||
| B、参加反应的氯气的物质的量等于3a mol | ||||||
| C、改变温度,反应中转移电子的物质的量ne的范围:3a mol<ne<5a mol | ||||||
| D、改变温度,产物中KClO3的最大理论产量为a mol |
 已知:4NH3+5O2
已知:4NH3+5O2