已知热化学方程式C2H2(g)+
O2(g)═2CO2(g)+H2O(g)△H=-1256kJ/mol,下列说法正确的是( )
| 5 |
| 2 |
| A、乙炔(C2H2)的燃烧热为1256 kJ/mol |
| B、若转移10 mol电子,则消耗2.5 mol O2 |
| C、若生成2 mol液态水,则△H=-2512 kJ/mol |
| D、若形成4 mol碳氧共用电子对,则放出的热量为2512 kJ |
下列化学方程式,能用离子方程式SO42-+Ba2+=BaSO4↓表示的是( )
| A、稀硫酸与氢氧化钡反应 |
| B、氢氧化钡与硫酸铜反应 |
| C、硫酸氢钠与少量氢氧化钡反应 |
| D、氯化钡与硫酸镁反应 |
下列离子方程式表达正确的是( )
| A、0.01mol/LNH4Al(SO4)2溶液与0.02mol/LBa(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3?H2O |
| B、氯气通入水中:Cl2+H2O=Cl-+ClO-+2H+ |
| C、Ca(HCO3)2溶液中滴加过量的NaOH溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| D、用氢氧化钠溶液除去铝表面的氧化膜:Al2O3+2OH-=2AlO2-+H2O |
设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A、1mol金刚石晶体中含碳碳键数为2NA |
| B、10.6g Na2CO3溶于水中CO32-的个数为0.1NA |
| C、标准状况下,22.4LSO3中含有的氧原子数为0.3 NA |
| D、1 mol Na2O2与足量CO2反应转移的电子数2NA |
已知H+(aq)+OH-(aq)=H2O (l);△H=-57.3KJ/mol.则下列热化学方程式正确的是( )
| A、CH3COOH(aq)+NaOH(aq)=CH3COONa (aq)+H2O(l);△H=-57.3KJ/mol |
| B、H2SO4(aq)+Ba(OH)2(aq)=BaSO4 (s)+2 H2O(l);△H=-114.6KJ/mol |
| C、HCl(aq)+NaOH(s)=NaCl (aq)+H2O(l);△H=-57.3KJ/mol |
| D、HI(aq)+KOH(aq)=KI(aq)+H2O(l);△H=-57.3KJ/mol |
将Fe片和Al片放在盛有NaCl溶液(其中滴入酚酞)的表面皿中,如图表示,最先观察到变红色的区域为( )
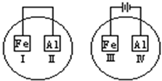

| A、II和Ⅳ | B、Ⅱ和Ⅲ |
| C、Ⅰ和Ⅲ | D、Ⅰ和Ⅳ |
下列叙述正确的是( )
| A、在原电池的负极和电解池的阴极上都是发生失电子的氧化反应 |
| B、用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1:2 |
| C、用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 molNaOH |
| D、电解精炼铜时,将粗铜作电解池的阴极,纯铜作电解池的阳极 |
下列化学用语表达不正确的是( )
A、次氯酸的电子式: | ||||
B、质子数为6、质量数为14的原子:
| ||||
| C、CS2的结构式:S-C-S | ||||
D、氯的原子结构示意图: |
下列有关化学用语表示正确的是( )
| A、氢的三种同位素:H2、D2、T2 |
B、F-的结构示意图: |
| C、中子数为20的氯原子:2017Cl |
D、NH3的电子式: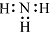 |