题目内容
下列有关化学用语表示正确的是( )
| A、氢的三种同位素:H2、D2、T2 |
B、F-的结构示意图: |
| C、中子数为20的氯原子:2017Cl |
D、NH3的电子式: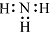 |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.同位素的研究对象为原子,是指同种元素的不同原子之间的互称;
B.氟离子的核电荷数为9,核外电子总数为10,最外层达到8电子稳定结构;
C.元素符号的左上角表示的质量数,该氯原子的质量数为:20+17=37,表示20;
D.氨气的电子式中漏掉了氮原子的1对未成键电子对.
B.氟离子的核电荷数为9,核外电子总数为10,最外层达到8电子稳定结构;
C.元素符号的左上角表示的质量数,该氯原子的质量数为:20+17=37,表示20;
D.氨气的电子式中漏掉了氮原子的1对未成键电子对.
解答:
解:A.H2、D2、T2都是氢气分子,为同一种物质,H、D、T为氢的同位素,故A错误;
B.氟离子的核电荷数为9,最外层达到8电子稳定结构,F-的结构示意图为: ,故B正确;
,故B正确;
C.氯元素的质子数为17,中子数为20的氯原子的质量数为37,该氯原子的正确表示方法为:1737Cl,故C错误;
D.氨气分子中存在3个氮氢键,氮原子最外层达到8电子稳定结构,氨气正确的电子式为: ,故D错误;
,故D错误;
故选B.
B.氟离子的核电荷数为9,最外层达到8电子稳定结构,F-的结构示意图为:
 ,故B正确;
,故B正确;C.氯元素的质子数为17,中子数为20的氯原子的质量数为37,该氯原子的正确表示方法为:1737Cl,故C错误;
D.氨气分子中存在3个氮氢键,氮原子最外层达到8电子稳定结构,氨气正确的电子式为:
 ,故D错误;
,故D错误;故选B.
点评:本题考查了常见化学用语的书写方法判断,题目难度中等,注意掌握电子式、离子结构示意图、同位素、元素符号等化学用语的概念及书写方法,选项D为易错点,注意不可漏掉N原子的未成键电子.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列关于强弱电解质的说法中,正确的是( )
| A、MgO在熔化状态下全部电离,是弱电解质 |
| B、具有极性键的共价化合物都是强电解质 |
| C、具有非极性键的共价化合物都是弱电解质 |
| D、所有弱酸、弱碱都是弱电解质 |
下列各溶液中一定能大量共存的离子组是( )
| A、加入铝粉有氢气生成的溶液中:Mg2+、Cu2+、SO42-、K+ |
| B、使pH试纸呈红色的溶液中:Fe2+、I-、NO3-、Cl- |
| C、常温下,c(H+)=10-14mol/L的溶液中:Na+、AlO2-、S2-、SO32- |
| D、常温下,水电离出的c(H+)与c(OH-)乘积为10-28的溶液中:K+、Na+、HCO3-、Ca2+ |
下列说法不正确的是( )
| A、两个原子之间形成共价键时,最多有一个σ键 |
| B、σ键比π键重叠程度大,形成的共价键强 |
| C、N2分子中有一个σ键,2个π键 |
| D、气体单质中,一定有σ键,可能有π键 |
用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气的生成速率加快的是( )
| A、通入HCl气体 |
| B、不用铁片,改用铁粉 |
| C、滴加少量硫酸铜溶液 |
| D、加入KNO3固体 |
已知H+(aq)+OH-(aq)=H2O (l);△H=-57.3KJ/mol.则下列热化学方程式正确的是( )
| A、CH3COOH(aq)+NaOH(aq)=CH3COONa (aq)+H2O(l);△H=-57.3KJ/mol |
| B、H2SO4(aq)+Ba(OH)2(aq)=BaSO4 (s)+2 H2O(l);△H=-114.6KJ/mol |
| C、HCl(aq)+NaOH(s)=NaCl (aq)+H2O(l);△H=-57.3KJ/mol |
| D、HI(aq)+KOH(aq)=KI(aq)+H2O(l);△H=-57.3KJ/mol |
下列各组中物质的俗称、学名与化学式表示同一种物质的是( )
| A、烧(火)碱 氢氧化钠 NaOH |
| B、纯碱 氢氧化钠 NaOH |
| C、熟石灰 氧化钙 CaO |
| D、铜绿 氢氧化铜 Cu2(OH)2CO3 |
下列说法正确的是( )
| A、纯净物只由一种元素组成,而混合物由两种或两种以上元素组成 |
| B、纯净物只由一种原子组成,而混合物由多种原子组成 |
| C、只由一种分子组成的物质一定为纯净物,组成混合物的物质可能只有一种元素 |
| D、只由一种元素的阳离子与另一种元素的阴离子组成的物质一定为纯净物 |