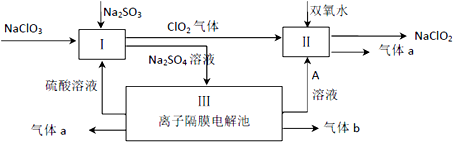
X、Y、Z、W、M五种元素的原子序数依次增大.已知X、Y、Z、W是短周期元素中的四种非金属元素,X元素的原子形成的离子就是一个质子,Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体,Y原子的最外层电子数是内层电子数的2倍. M是地壳中含量最高的金属元素.下列说法正确的是( )
| A、五种元素的原子半径从大到小的顺序是:M>W>Z>Y>X |
| B、化合物X2W2、YW2、ZW、ZW2等都含有极性共价键,但都属于非极性分子 |
| C、用M单质作阳极,石墨电极作阴极电解NaHCO3溶液,电解一段时后,在阴极区会出现白色沉淀 |
| D、X、Z两元素能形成原子个数比(X:Z)为3:1和4:2的化合物 |
下列说法不正确的是( )
| A、工业上冶炼Fe用热还原方法 |
| B、海水淡化的方法主要有蒸馏法,电渗析法,离子交换法等 |
| C、工业上通过煤的干馏可获得芳香烃 |
| D、单质硅是将太阳能转变为电能的材料,二氧化硅可以做半导体材料 |
溴化碘(IBr)的化学性质很像卤素的单质,它能与大多数金属、非金属化合生成卤化物,它也能与水发生以下反应:IBr+H2O→HBr+HIO,下列有关IBr的叙述中,不正确的是( )
| A、在很多反应中IBr是强氧化剂 |
| B、IBr与水反应时既做氧化剂,又做还原剂 |
| C、IBr与AgNO3溶液反应会生成AgBr沉淀 |
| D、IBr与NaOH溶液反应时,生成NaBr和NaIO |
以下对实验操作的说法正确的是( )
| A、由于合金中金属的活泼性不同所以合金都易生锈 |
| B、进行焰色反应时,所用铂丝先用NaOH溶液洗涤并充分灼烧 |
| C、配制FeCl3溶液时,应将FeCl3溶解在适量的HCl中 |
| D、酸碱中和滴定时,锥形瓶需用待测液润洗2遍,再加入待测液 |
氯、溴、碘等卤族元素主要来自海水,很多海洋植物中都含有大量的碘,反应①是从海藻灰中提取碘的主要反应,反应②是从智利硝石中提取碘的主要反应:2NaI+MnO2+3H2SO4═2NaHSO4+MnSO4+2H2O+I2 ①
2NaIO3+5NaHSO3═2Na2SO4+3NaHSO4+H2O+I2②下列有关说法正确的是( )
2NaIO3+5NaHSO3═2Na2SO4+3NaHSO4+H2O+I2②下列有关说法正确的是( )
| A、NaI和NaIO3在一定条件下能反应生成I2 |
| B、I2在反应①中是还原产物,在反应②中是氧化产物 |
| C、两个反应中生成等量的I2时转移电子数相等 |
| D、氧化性:Mn02>SO42->I03->I2 |
下列叙述不正确的是( )
| A、纯银器表面在空气中因化学腐蚀渐渐变暗 |
| B、氢氧燃料电池是一种将化学能转化为电能的装置 |
| C、可用浸有酸性高锰酸钾溶液的滤纸来检验二氧化硫气体的漂白性 |
| D、塑料袋在全球“失宠”,有偿使用成为风尚,是因为塑料袋填埋占用土地,且难以降解 |
已知可用MnO2制备Cl2,下列叙述不正确的是( )
| A、氧化产物为Cl2 |
| B、氧化剂与还原剂的物质的量之比为1:4 |
| C、若有1mol Cl2生成,则反应中有2mol电子转移 |
| D、微粒的氧化性 Cl2>MnO2 |
NaCl是一种化工原料,可以制备一系列物质(如图).下列说法正确的是( )
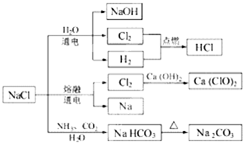

| A、25℃,NaHCO3在水中的溶解度比Na2CO3的大 |
| B、石灰乳与Cl2的反应中,Cl2是氧化剂,Ca(OH)2是还原剂 |
| C、常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 |
| D、如图所示转化反应中有4个反应属于氧化还原反应 |