题目内容
氯、溴、碘等卤族元素主要来自海水,很多海洋植物中都含有大量的碘,反应①是从海藻灰中提取碘的主要反应,反应②是从智利硝石中提取碘的主要反应:2NaI+MnO2+3H2SO4═2NaHSO4+MnSO4+2H2O+I2 ①
2NaIO3+5NaHSO3═2Na2SO4+3NaHSO4+H2O+I2②下列有关说法正确的是( )
2NaIO3+5NaHSO3═2Na2SO4+3NaHSO4+H2O+I2②下列有关说法正确的是( )
| A、NaI和NaIO3在一定条件下能反应生成I2 |
| B、I2在反应①中是还原产物,在反应②中是氧化产物 |
| C、两个反应中生成等量的I2时转移电子数相等 |
| D、氧化性:Mn02>SO42->I03->I2 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:①2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+2H2O+I2中,I元素由-1价升高为0,Mn元素由+4价降低为+2价;
②2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2中,I元素的化合价由+5价降低为0,S元素的化合价由+4价升高为+6价,以此来解答.
②2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2中,I元素的化合价由+5价降低为0,S元素的化合价由+4价升高为+6价,以此来解答.
解答:
解:①2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+2H2O+I2中,I元素由-1价升高为0,Mn元素由+4价降低为+2价;
②2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2中,I元素的化合价由+5价降低为0,S元素的化合价由+4价升高为+6价,
A.NaI具有还原性,NaIO3具有氧化性,则NaI和NaIO3在一定条件下能反应生成I2,故A正确;
B.反应①中碘元素的化合价升高,反应②中碘元素的化合价降低,则I2在反应①中是氧化产物,在反应②中是还原产物,故B错误;
C.生成1molI2时,反应①转移2mol电子,反应②转移10mol电子,故C错误;
D.由反应②可知氧化性I03->SO42-,故D错误.
故选A.
②2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2中,I元素的化合价由+5价降低为0,S元素的化合价由+4价升高为+6价,
A.NaI具有还原性,NaIO3具有氧化性,则NaI和NaIO3在一定条件下能反应生成I2,故A正确;
B.反应①中碘元素的化合价升高,反应②中碘元素的化合价降低,则I2在反应①中是氧化产物,在反应②中是还原产物,故B错误;
C.生成1molI2时,反应①转移2mol电子,反应②转移10mol电子,故C错误;
D.由反应②可知氧化性I03->SO42-,故D错误.
故选A.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化是解答本题的关键,注意利用化合价计算转移的电子数,题目难度不大.

练习册系列答案
相关题目
分子中碳与氢两元素的质量比为21:4的烃中主链上有5个碳原子的结构共有( )
| A、3种 | B、4种 | C、5种 | D、6种 |
Al与重氢氧化钠(NaOD)的水溶液反应,其中水中不含重氢.下列说法正确的是( )
| A、生成的氢气中只含有H2 |
| B、生成的氢气中只含有D2 |
| C、生成的氢气中含有H2、HD、D2 |
| D、以上判断都不正确 |
X、Y、Z、W、M五种元素的原子序数依次增大.已知X、Y、Z、W是短周期元素中的四种非金属元素,X元素的原子形成的离子就是一个质子,Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体,Y原子的最外层电子数是内层电子数的2倍. M是地壳中含量最高的金属元素.下列说法正确的是( )
| A、五种元素的原子半径从大到小的顺序是:M>W>Z>Y>X |
| B、化合物X2W2、YW2、ZW、ZW2等都含有极性共价键,但都属于非极性分子 |
| C、用M单质作阳极,石墨电极作阴极电解NaHCO3溶液,电解一段时后,在阴极区会出现白色沉淀 |
| D、X、Z两元素能形成原子个数比(X:Z)为3:1和4:2的化合物 |
人类生活离不开化学知识,下列叙述不正确的是( )
| A、臭氧是饮用水的理想消毒剂之一,因为它杀菌能力强且不影响水质 |
| B、因患“禽流感”而被捕杀的家禽尸体常用生石灰处理 |
| C、医疗上常用体积分数为75%的酒精进行皮肤消毒 |
| D、食品加工、消毒、防腐常使用福尔马林 |
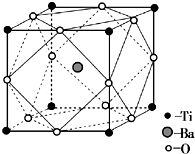 钛被誉为“未来世纪的金属”.试回答下列问题:
钛被誉为“未来世纪的金属”.试回答下列问题: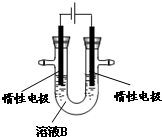 据报道,有一种叫Thibacillus Ferroxidans 的细菌在氧气存在下的酸性溶液中,能将黄铜矿(CuFeS2)氧化成硫酸盐,发生的反应为:
据报道,有一种叫Thibacillus Ferroxidans 的细菌在氧气存在下的酸性溶液中,能将黄铜矿(CuFeS2)氧化成硫酸盐,发生的反应为: