题目内容
以下对实验操作的说法正确的是( )
| A、由于合金中金属的活泼性不同所以合金都易生锈 |
| B、进行焰色反应时,所用铂丝先用NaOH溶液洗涤并充分灼烧 |
| C、配制FeCl3溶液时,应将FeCl3溶解在适量的HCl中 |
| D、酸碱中和滴定时,锥形瓶需用待测液润洗2遍,再加入待测液 |
考点:金属腐蚀的化学原理,焰色反应,溶液的配制,中和滴定
专题:实验评价题
分析:A.合金不一定易生锈;
B.焰色反应时,洗涤铂丝的洗涤液是稀盐酸;
C.氯化铁易水解生成氢氧化铁和HCl;
D.酸碱中和滴定时,锥形瓶不能用待测液润洗,但滴定管必须用标准液润洗.
B.焰色反应时,洗涤铂丝的洗涤液是稀盐酸;
C.氯化铁易水解生成氢氧化铁和HCl;
D.酸碱中和滴定时,锥形瓶不能用待测液润洗,但滴定管必须用标准液润洗.
解答:
解:A.合金不一定易生锈,如生铁易生锈是因为易形成原电池,不锈钢不易生锈是因为改变金属内部结构,故A错误;
B.焰色反应时,洗涤铂丝的洗涤液是稀盐酸,盐酸和部分物质反应生成的氯化物熔点低且稀盐酸易挥发,所以用稀盐酸作洗涤液,故B错误;
C.氯化铁易水解生成氢氧化铁和HCl,为防止氯化铁水解,应该将FeCl3溶解在适量的HCl中,故C正确;
D.酸碱中和滴定时,锥形瓶不能用待测液润洗,但滴定管必须用标准液润洗,否则易导致产生误差,故D错误;
故选C.
B.焰色反应时,洗涤铂丝的洗涤液是稀盐酸,盐酸和部分物质反应生成的氯化物熔点低且稀盐酸易挥发,所以用稀盐酸作洗涤液,故B错误;
C.氯化铁易水解生成氢氧化铁和HCl,为防止氯化铁水解,应该将FeCl3溶解在适量的HCl中,故C正确;
D.酸碱中和滴定时,锥形瓶不能用待测液润洗,但滴定管必须用标准液润洗,否则易导致产生误差,故D错误;
故选C.
点评:本题考查实验基本操作,明确物质的性质及实验原理是解本题关键,侧重考查学生分析问题、实验操作能力,D为易错选项,注意用容量瓶配制溶液、酸碱中和滴定中锥形瓶、用pH试纸测溶液pH都不能润洗或润湿,为易错点.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
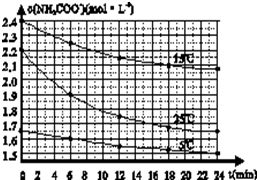 某研究性活动小组在实验室用三份不同初始浓度的氨基甲酸铵(NH2COONH4)溶液在不同温度下进行水解实验:NH2COONH4+2H2O?NH4HCO3+NH3?H2O,经测得c(NH2COO-)与反应时间的关系如图所示.据图判断下列说法正确的是( )
某研究性活动小组在实验室用三份不同初始浓度的氨基甲酸铵(NH2COONH4)溶液在不同温度下进行水解实验:NH2COONH4+2H2O?NH4HCO3+NH3?H2O,经测得c(NH2COO-)与反应时间的关系如图所示.据图判断下列说法正确的是( )| A、0~12 min,初始浓度越大的实验,水解反应速率越大 |
| B、c(NH2COO-)将随反应时间的不断延长而一直减小至0 |
| C、25℃时0~6 min,v(NH2COO-)为0.05 mol?L-1?min-1 |
| D、15℃时,第30 min时,c(NH2COO-)为2.0 mol?L-1 |
分析下表中各项的排布规律,按此规律排布对第29项X有关说法中不正确的是( )
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | … | 29 |
| C2H6 | C2H6O | C2H4O2 | C3H8 | C3H8O | C3H6O2 | C4H10 | … | X |
| A、X的分子式为C11H24O |
| B、X可能与金属钠反应生成氢气 |
| C、X可能与碳酸钠反应放出CO2气体 |
| D、X可能与第30项发生酯化反应 |
NaCl是一种化工原料,可以制备一系列物质(如图).下列说法正确的是( )
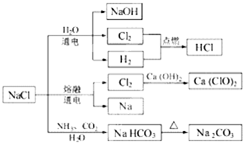

| A、25℃,NaHCO3在水中的溶解度比Na2CO3的大 |
| B、石灰乳与Cl2的反应中,Cl2是氧化剂,Ca(OH)2是还原剂 |
| C、常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 |
| D、如图所示转化反应中有4个反应属于氧化还原反应 |
下列说法中正确的是( )
| A、合成纤维和光导纤维都是新型无机非金属材料 |
| B、乙醛、氯乙烯和乙二醇均可作为合成聚合物的单体 |
| C、淀粉、纤维素的化学式都可表示为(C6H10O5)n,二者互为同分异构体 |
| D、乙醛、乙酸和葡萄糖都能与新制的Cu(OH)2反应,且反应类型均为氧化反应 |
化学与社会、环境密切相关,下列有关说法正确的是( )
| A、绿色化学的核心是应用化学原理对环境污染进行治理 |
| B、氯气和氢氧化钠溶液和石灰乳得到的含氯化合物都具有漂白性 |
| C、高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强碱会“断路” |
| D、对“地沟油”蒸馏可以获得汽油 |
下列有关化学用语中正确的是( )
| A、次氯酸分子的结构式:H-O-Cl |
B、聚丙烯的结构简式为: |
C、氮分子的结构式: |
D、丙烷分子的比例模型: |