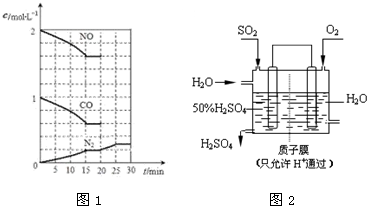
题目内容
X、Y、Z、W、M五种元素的原子序数依次增大.已知X、Y、Z、W是短周期元素中的四种非金属元素,X元素的原子形成的离子就是一个质子,Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体,Y原子的最外层电子数是内层电子数的2倍. M是地壳中含量最高的金属元素.下列说法正确的是( )
| A、五种元素的原子半径从大到小的顺序是:M>W>Z>Y>X |
| B、化合物X2W2、YW2、ZW、ZW2等都含有极性共价键,但都属于非极性分子 |
| C、用M单质作阳极,石墨电极作阴极电解NaHCO3溶液,电解一段时后,在阴极区会出现白色沉淀 |
| D、X、Z两元素能形成原子个数比(X:Z)为3:1和4:2的化合物 |
考点:原子结构与元素的性质
专题:
分析:X元素的原子形成的离子就是一个质子,故X为H,Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体,且为短周期非金属元素,原子序数依次增大Z为N,W为O,Y原子的最外层电子数是内层电子数的2倍所以Y为C,M是地壳中含量最高的金属元素,所以M是Al.
解答:
解:A.五种元素的原子半径从大到小的顺序是:M>Y>Z>W>X,故A错误;
B.NO该分子中的正负电荷重心不重合,是极性分子,故B错误;
C.电解时氢氧根阴离子向阳极移动,在阳极区会出现白色沉淀,故C错误;
D.X、Z两元素分别为H、N元素,可形成氨气和N2H4,故D正确.
故选D.
B.NO该分子中的正负电荷重心不重合,是极性分子,故B错误;
C.电解时氢氧根阴离子向阳极移动,在阳极区会出现白色沉淀,故C错误;
D.X、Z两元素分别为H、N元素,可形成氨气和N2H4,故D正确.
故选D.
点评:本题考查结构性质位置关系应用,正确推断元素是解本题关键,难度不大,注意对基础知识的掌握.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列叙述正确的是( )
| A、0.1mol/L NaHCO3溶液中:c(H+)+c(Na+)=c(OH-)+c(HCO3-)+c(CO32-) |
B、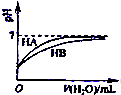 表示常温下,稀释HA、HB两种酸的稀溶液时,溶液PH随加水量的变化,则NaA溶液的PH大于同浓度的NaB溶液的PH |
C、 表示在其他条件相同时,分别在T1、T2温度下由CO2和H2合成甲醇的物质的量随时间变化情况,则CO2和H2合成甲醇是放热反应 |
D、 表示将1.000 mol/L氨水滴入20.00mL1.000 mol/L盐酸中,溶液PH和温度随加入氨水体积变化曲线 |
下列关于常见有机物的说法中,不正确的是( )
| A、甲烷、苯、乙醇和乙酸在一定条件下都能发生取代反应 |
| B、乙烯使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色的反应类型不同 |
| C、塑料、合成橡胶、合成纤维都属于合成有机高分子材料 |
| D、化学式均为(C6H10O5)n的淀粉和纤维素互为同分异构体 |
氯、溴、碘等卤族元素主要来自海水,很多海洋植物中都含有大量的碘,反应①是从海藻灰中提取碘的主要反应,反应②是从智利硝石中提取碘的主要反应:2NaI+MnO2+3H2SO4═2NaHSO4+MnSO4+2H2O+I2 ①
2NaIO3+5NaHSO3═2Na2SO4+3NaHSO4+H2O+I2②下列有关说法正确的是( )
2NaIO3+5NaHSO3═2Na2SO4+3NaHSO4+H2O+I2②下列有关说法正确的是( )
| A、NaI和NaIO3在一定条件下能反应生成I2 |
| B、I2在反应①中是还原产物,在反应②中是氧化产物 |
| C、两个反应中生成等量的I2时转移电子数相等 |
| D、氧化性:Mn02>SO42->I03->I2 |
如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )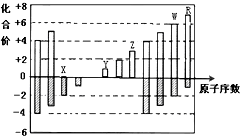

| A、原子半径:Z>Y>X |
| B、气态氢化物的稳定性:W>R |
C、X的一种氢化物具有氧化性,其电子式为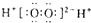 |
| D、Y和Z两者最高价氧化物对应的水化物能相互反应 |
X、Y、Z、W是原子序数依次递增的四种短周期元素,甲、乙、丙、丁是它们两两组合而形成的化合物,且能发生反应:甲+乙→丙+丁,乙、丙、丁的化学式分别为Y2Z、YW2、ZX4,丁是一种常见的液体溶剂,0.1mol/L甲的水溶液的pH为1(25℃).下列说法正确的是( )
| A、原子半径:W>Z>Y>X |
| B、Z元素在周期表的位置为第三周期第ⅡA族 |
| C、丁的稳定性小于甲烷 |
| D、丙的水溶液呈碱性 |
NA表示阿伏加德罗常数值.下列说法正确的是( )
| A、1mol Na2O2与足量CO2充分反应转移的电子数为2NA |
| B、常温下,pH=1的醋酸溶液中,醋酸分子的数目一定大于0.1NA |
| C、向FeI2溶液中通入适量氯气,当有1molFe2+被氧化时,总共转移电子的数目为NA |
| D、t℃时,1L pH=6的纯水中,含1×10-6 NA个OH- |
(A 做)将100mL2.0mol/L的Na2SO4和300mL2.0mol/L的AI2(SO4)3的溶液混合,则混合溶液中SO42-的物质的量浓度约为(假设溶液的体积可以相加)( )
| A、6.0g/mol |
| B、5.0g/mol |
| C、10.0g/mol |
| D、4.0g/mol |