下列说法正确的是( )
| A、非金属元素组成的化合物中只可能含有共价键 |
| B、ⅦA族元素气态氢化物的热稳定性和还原性从上到下依次减弱 |
| C、第三周期非金属元素最高价含氧酸的酸性从左到右依次增强 |
| D、元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |
如图是部分短周期元素最外层电子数与原子序数的关系图,下列说法正确的是( )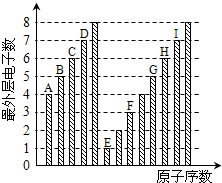

| A、原子半径:A<B<C<D |
| B、E和C元素形成的化合物中只可能存在离子键 |
| C、气态氢化物稳定性:I>D>H>G |
| D、E、F和H三种元素相应的最高价氧化物对应水化物之间两两会发生反应 |
X、Y、Z、W为原子序数依次增大的短周期元素.其形成的小分子化合物Y2X2、Z2X4、X2W2中,相应分子内各原子最外层电子都满足稳定结构.下列说法正确的是( )
| A、X、Y、Z、W的原子半径的大小关系为:W>Y>Z>X |
| B、在化合物Y2X2、Z2X4、X2W2中,分子所含的共用电子对数相等 |
| C、与元素Y、Z相比,元素W形成的简单氢化物最稳定,是因为其分子间存在氢键 |
| D、X、Y、Z、W四种元素可形成化学式为X7Y2ZW2的有机物 |
下列有关电化学原理的说法正确的是( )
| A、电解法冶炼铝时,阳极反应为:2O2--4e-=O2↑ |
| B、用电解法精练铜,阳极反应为:Cu2++2e-=Cu |
| C、钢铁在中性条件下被腐蚀,正极反应为:2H2O+2e-=H2↑+2OH- |
| D、铝-空气燃料电池以KOH为电解液时,负极反应为:Al-3e-=Al3+ |
 关于下列各图的叙述不正确的是( )
关于下列各图的叙述不正确的是( )| 表 丙 | |
| 化学方程式 | 平衡常数K |
| F2+H2?2HF | 6.5×1095 |
| Cl2+H2=2HCl | 2.6×1033 |
| Br2+H2?2HBr | 1.9×1019 |
| I2+H2?2HI | 8.7×102 |
| A、已知1molCO燃烧放出的热为283kJ,2H2(g)+O2(g)=2H2O(g);△H=-483.6kJ/mol则图甲表示CO和H2O(g)生成CO2和H2的能量变化 | ||
| B、某温度下,pH=11的NH3?H2O和pH=1的盐酸等体积混合后(不考虑混合后溶液体积的变化)恰好完全反应,反应后的溶液中NH4+、NH3?H2O与NH3三种微粒的平衡浓度之和为0.045mol?Lˉ1 | ||
| C、在常温下,X2(g)和H2反应生成HX的平衡常数如表丙所示,仅依据K的变化,就可以说明在相同条件下,平衡时X2(从F2到I2)的转化率逐减小,且X2与H2反应的剧烈程度逐渐减弱 | ||
D、图乙中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中,
|
有下列三个反应:下列说法正确的是( )
①Cl2+FeI2═FeCl2+I2
②2Fe2++Br2═2Fe3++2Br-
③Co2O3+6HCl═2CoCl2+Cl2↑+3H2O.
①Cl2+FeI2═FeCl2+I2
②2Fe2++Br2═2Fe3++2Br-
③Co2O3+6HCl═2CoCl2+Cl2↑+3H2O.
| A、反应①②③中的氧化产物分别是I2、Fe3+、CoCl2 |
| B、根据以上方程式可以得到氧化性:Cl2>Fe3+>Co2O3 |
| C、在反应③中当1 mol Co2O3参加反应时,2 mol HCl被氧化 |
| D、可以推理得到Cl2+FeBr2═FeCl2+Br2 |
按图装置进行实验,下列描述正确的是(N装置中两个电极均为石墨棒)( )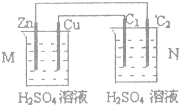

| A、C1上发生还原反应 |
| B、M装置中SO2-4移向Cu电极 |
| C、工作一段时间后装置M中溶液PH变大,装置N中溶液PH变小 |
| D、Cu电极与C2电极上的电极反应不同 |
如图为阳离子交换膜法电解饱和食盐水原理示意图.下列说法不正确的是( )
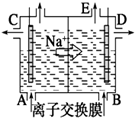

| A、完全电解后加适量盐酸可以恢复到电解前的浓度 |
| B、从B中加入含少量NaOH的水溶液以增强导电性 |
| C、标准状况下每生成22.4 L Cl2,使产生2 mol NaOH |
| D、从E口逸出的气体是H2 |
下列有关说法正确的是( )
| A、室温下反应C(s)+CO2(g)=2CO(g)不能自发进行,说明其△H<0 |
| B、25℃时PH=5的盐酸和PH=9的氨水,两溶液中水的电离程度不同 |
| C、25℃时Ksp(A)>Ksp(B),说明化合物A的溶解度比化合物B的大 |
| D、在NH4Cl溶液中加入适量的硫酸,可使c(NH4+):c(Cl-)接近1:1 |
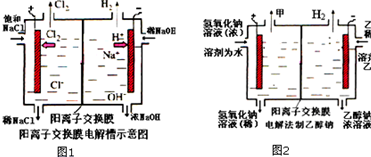 工业上生产氯气,常用电解槽电解饱和食盐水,为了避免电解产物之间发生反应,常用阳离子交换膜将电解槽隔成两部分.如图1为电解槽的示意图.
工业上生产氯气,常用电解槽电解饱和食盐水,为了避免电解产物之间发生反应,常用阳离子交换膜将电解槽隔成两部分.如图1为电解槽的示意图.