题目内容
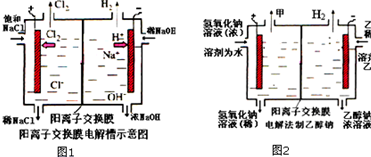 工业上生产氯气,常用电解槽电解饱和食盐水,为了避免电解产物之间发生反应,常用阳离子交换膜将电解槽隔成两部分.如图1为电解槽的示意图.
工业上生产氯气,常用电解槽电解饱和食盐水,为了避免电解产物之间发生反应,常用阳离子交换膜将电解槽隔成两部分.如图1为电解槽的示意图.(1)这种阳离子交换膜,只允许溶液中的
①H2 ②Cl2 ③H+ ④Cl- ⑤Na+ ⑥OH-
(2)某化学课外兴趣小组设计了用电解法制取乙醇钠的工业方法,所用的电解槽如图2所示,设计要求:①所用的交换膜不能让分子自由通过;②电解过程中消耗的原料是氢氧化钠和乙醇.回答下列问题:
①写出在电解过程中发生的电极方程式阴极:
②最后从乙醇钠的乙醇溶液中分离得到纯净乙醇钠固体的方法是:
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)阳离子交换膜只允许阳离子通过,而阴离子、分子不能通过;
(2)①电解池中和电源的负极相连的是电解池的阴极,发生得电子的还原反应;
②从溶液中析出溶质的方法是蒸发结晶,可类比食盐的蒸发结晶.
(2)①电解池中和电源的负极相连的是电解池的阴极,发生得电子的还原反应;
②从溶液中析出溶质的方法是蒸发结晶,可类比食盐的蒸发结晶.
解答:
解:(1)阳离子交换膜只允许阳离子钠离子、氢离子通过,而阴离子和分子均不能通过,故答案为:③⑤;
(2)①电解池中和电源的负极相连的是电解池的阴极,阴极上乙醇得电子发生还原反应,即2CH3CH2OH+2e-=2CH3CH2O-+H2↑.
故答案为:2CH3H2OH+2e-=2CH3CH2O-+H2↑;
②从溶液中析出溶质的方法是蒸发结晶,故答案为:蒸发结晶.
(2)①电解池中和电源的负极相连的是电解池的阴极,阴极上乙醇得电子发生还原反应,即2CH3CH2OH+2e-=2CH3CH2O-+H2↑.
故答案为:2CH3H2OH+2e-=2CH3CH2O-+H2↑;
②从溶液中析出溶质的方法是蒸发结晶,故答案为:蒸发结晶.
点评:本题考查了电解原理、电极反应式书写、混合物分离等知识点,难度不大.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
两种气态烃组成的混合气体0.1mol,完全燃烧得0.16molCO2和3.6g水.下列说法正确的是( )
| A、混合气体一定没有甲烷 |
| B、混合气体中一定是甲烷和乙烯 |
| C、混合气体中一定没有乙烷 |
| D、混合气体中一定有乙烯 |
下列说法正确的是( )
| A、食用加碘盐可预防碘缺乏症,加碘盐中加的含碘物质是碘单质 |
| B、因为NaCl的水溶液能导电,所以NaCl溶液属于强电解质 |
| C、电解熔融NaCl得到23.0g金属钠时能产生22.4 L氯气(标准状况下) |
| D、37Cl 是氯元素的一种同位素,23Na37Cl中质子数和中子数之比是7:8 |
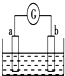 如图所示,两电极一为碳棒,一为铁片,若电流表的指针发生偏转,且a极上有大量气泡生成,则以下叙述正确的是( )
如图所示,两电极一为碳棒,一为铁片,若电流表的指针发生偏转,且a极上有大量气泡生成,则以下叙述正确的是( )| A、a为负极,是铁片,烧杯中的溶液为稀硫酸 |
| B、b为负极,是铁片,烧杯中的溶液为硫酸铜溶液 |
| C、a为正极,是碳棒,烧杯中的溶液为稀硫酸 |
| D、b为正极,是碳棒,烧杯中的溶液为硫酸铜溶液 |
 关于下列各图的叙述不正确的是( )
关于下列各图的叙述不正确的是( )| 表 丙 | |
| 化学方程式 | 平衡常数K |
| F2+H2?2HF | 6.5×1095 |
| Cl2+H2=2HCl | 2.6×1033 |
| Br2+H2?2HBr | 1.9×1019 |
| I2+H2?2HI | 8.7×102 |
| A、已知1molCO燃烧放出的热为283kJ,2H2(g)+O2(g)=2H2O(g);△H=-483.6kJ/mol则图甲表示CO和H2O(g)生成CO2和H2的能量变化 | ||
| B、某温度下,pH=11的NH3?H2O和pH=1的盐酸等体积混合后(不考虑混合后溶液体积的变化)恰好完全反应,反应后的溶液中NH4+、NH3?H2O与NH3三种微粒的平衡浓度之和为0.045mol?Lˉ1 | ||
| C、在常温下,X2(g)和H2反应生成HX的平衡常数如表丙所示,仅依据K的变化,就可以说明在相同条件下,平衡时X2(从F2到I2)的转化率逐减小,且X2与H2反应的剧烈程度逐渐减弱 | ||
D、图乙中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中,
|
某课外兴趣小组通过实验发现钾和钠的化学性质相似,下列说法中能最恰当地解释这个事实的是( )
| A、都是金属元素 |
| B、原子半径相差不大 |
| C、原子结构相似,最外层电子数相同 |
| D、最高化合价相同 |
化学与生活密切相关.下列说法中不正确的是( )
| A、塑料、橡胶、纤维都是有机高分子化合物 |
| B、核电站泄露的放射性物质131I和127I互为同位素,化学性质相似 |
| C、以NO和NO2为主的氮氧化物是形成光化学烟雾和酸雨的一个重要原因 |
| D、氢氧化铁胶体、含PM2.5(是指大气中直径接近于2.5×10-5m的细颗粒物)的大气均具有丁达尔效应 |