题目内容
X、Y、Z、W为原子序数依次增大的短周期元素.其形成的小分子化合物Y2X2、Z2X4、X2W2中,相应分子内各原子最外层电子都满足稳定结构.下列说法正确的是( )
| A、X、Y、Z、W的原子半径的大小关系为:W>Y>Z>X |
| B、在化合物Y2X2、Z2X4、X2W2中,分子所含的共用电子对数相等 |
| C、与元素Y、Z相比,元素W形成的简单氢化物最稳定,是因为其分子间存在氢键 |
| D、X、Y、Z、W四种元素可形成化学式为X7Y2ZW2的有机物 |
考点:原子结构与元素周期律的关系
专题:
分析:在化合物Y2X2、Z2X4、X2W2中,相应分子内各原子最外层电子都满足稳定结构,X应为H,形成的化合物分别为C2H2、N2H4、H2O2,则Y为C,Z为N,W为O,以此解答该题.
解答:
解:在化合物Y2X2、Z2X4、X2W2中,相应分子内各原子最外层电子都满足稳定结构,X应为H,形成的化合物分别为C2H2、N2H4、H2O2,则Y为C,Z为N,W为O,
A.X、Y、Z、W的原子半径的大小关系为C(Y)>N(Z)>W(O)>X(H),故A错误;
B.在化合物C2H2、N2H4、H2O2中,含有的电子对数分别为5、5、3,不相等,故B错误;
C.氢化物的稳定性与氢键无关,与共价键的强弱有关,故C错误;
D.X、Y、Z、W四种元素可形成化学式为H7C2NO2的化合物,为CH2OH-CH(OH)NH2,故D正确.
故选D.
A.X、Y、Z、W的原子半径的大小关系为C(Y)>N(Z)>W(O)>X(H),故A错误;
B.在化合物C2H2、N2H4、H2O2中,含有的电子对数分别为5、5、3,不相等,故B错误;
C.氢化物的稳定性与氢键无关,与共价键的强弱有关,故C错误;
D.X、Y、Z、W四种元素可形成化学式为H7C2NO2的化合物,为CH2OH-CH(OH)NH2,故D正确.
故选D.
点评:本题考查原子结构与元素周期律的关系,题目难度中等,注意把握元素周期律的递变规律以及原子核外电子的排布特点,明确元素的种类为解答该题的关键.

练习册系列答案
相关题目
下列关于有机物的叙述正确的是( )
| A、我国居民传统膳食以糖类为主,淀粉、脂肪都是糖类物质 |
| B、人体内的蛋白质不断分解,最终生成水和二氧化碳排出体外 |
| C、乙醇可以被氧化为乙酸,二者均能发生酯化反应 |
| D、用氢氧化钠溶液可除去乙酸乙酯中混有的少量的乙酸 |
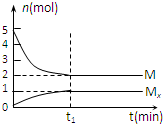 E是非金属性最强的元素,M是E的气态氢化物,在一定体积的密闭容器中,气体M存在如下关系:aM(g)?bMx(g ),反应物和生成物的物质的量随时间的变化关系如图.下列说法正确的是( )
E是非金属性最强的元素,M是E的气态氢化物,在一定体积的密闭容器中,气体M存在如下关系:aM(g)?bMx(g ),反应物和生成物的物质的量随时间的变化关系如图.下列说法正确的是( )| A、该反应的化学方程式是2HF?(HF)2 |
| B、时刻,保持温度不变,再充入5molM,重新达到平衡时,将减小 |
| C、平衡时混合气体的平均摩尔质量是33.3g/mol |
| D、M的沸点比同主族下一周期元素的气态氢化物沸点低 |
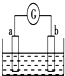 如图所示,两电极一为碳棒,一为铁片,若电流表的指针发生偏转,且a极上有大量气泡生成,则以下叙述正确的是( )
如图所示,两电极一为碳棒,一为铁片,若电流表的指针发生偏转,且a极上有大量气泡生成,则以下叙述正确的是( )| A、a为负极,是铁片,烧杯中的溶液为稀硫酸 |
| B、b为负极,是铁片,烧杯中的溶液为硫酸铜溶液 |
| C、a为正极,是碳棒,烧杯中的溶液为稀硫酸 |
| D、b为正极,是碳棒,烧杯中的溶液为硫酸铜溶液 |
如图为阳离子交换膜法电解饱和食盐水原理示意图.下列说法不正确的是( )
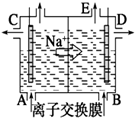

| A、完全电解后加适量盐酸可以恢复到电解前的浓度 |
| B、从B中加入含少量NaOH的水溶液以增强导电性 |
| C、标准状况下每生成22.4 L Cl2,使产生2 mol NaOH |
| D、从E口逸出的气体是H2 |
某课外兴趣小组通过实验发现钾和钠的化学性质相似,下列说法中能最恰当地解释这个事实的是( )
| A、都是金属元素 |
| B、原子半径相差不大 |
| C、原子结构相似,最外层电子数相同 |
| D、最高化合价相同 |
NA代表阿伏加德罗常数,下列说法不正确的是( )
| A、标准状况下,11.2L氯仿(CHCl3)中含有C-Cl键的数目为1.5NA |
| B、常温常压下,15g甲基(-CH3)所含的电子数为9NA |
| C、同温同压下,1LNO和1LO2充分混合体积小于1.5L |
| D、pH=l的醋酸溶液100mL中氢离子数为0.01 NA |
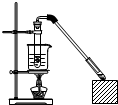 乙酸和乙醇反应的装置如图所示:在试管里加入3mL乙醇,然后一边摇动,一边慢慢地加入2mL浓硫酸和2mL冰醋酸,用酒精灯小心均匀地加热10min,将产生的蒸气经长导管通入到小试管中溶液的液面上.
乙酸和乙醇反应的装置如图所示:在试管里加入3mL乙醇,然后一边摇动,一边慢慢地加入2mL浓硫酸和2mL冰醋酸,用酒精灯小心均匀地加热10min,将产生的蒸气经长导管通入到小试管中溶液的液面上.