已知:H2(g)+
O2(g)═H2O(g);△H=-Q1 kJ?mol-12H2(g)+O2(g)═2H2O(l);△H=-Q2 kJ?mol-1则下列判断正确的是( )
| 1 |
| 2 |
| A、2Q1>O2 | ||
| B、Q1>2Q2 | ||
| C、2Q1<Q2 | ||
D、
|
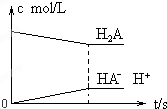
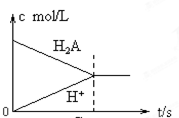
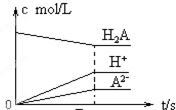
欲使醋酸溶液中的CH3COO-浓度增大,电离平衡向右移动,且不放出气体,可向醋酸溶液中加入少量固体( )
| A、NaOH |
| B、NaHCO3 |
| C、CH3COOK |
| D、Mg |
在2L密闭容器中加入或通入一定量A、B、C三种物质,在一定条件下发生反应(如图1),3min后给体系加热,气体C的体积分数Ψ(C)和混合气体的平均相对分子质量M均随温度分别发生了图示变化(如图2、图3).下列有关说法不正确的是( )
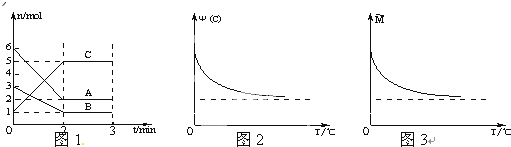

| A、前2min中C的平均反应速率为1mol/L?min |
| B、该反应的化学方程式为:2A+B?2C |
| C、正反应是放热反应 |
| D、A、B一定均为气态 |
在同温同压下,下列各组热化学方程式中 Q1<Q2的是(反应条件已略去)( )
| A、2H2(g)+O2(g)=2H2O(l);△H=-Q1,2H2(g)+O2(g)=2H2O (g);△H=-Q2 | ||||
| B、S(g)+O2(g)=SO2(g);△H=-Q1,S(s)+O2(g)=SO2(g);△H=-Q2 | ||||
C、C(s)+
| ||||
D、H2(g)+Cl2(g)=2HCl(g);△H=-Q1,
|
可逆反应A(g)+B?C(g)+D,达到平衡时,下列说法不正确的是( )
| A、若B是气体,增大A的浓度会使B转化率增大 |
| B、若增大A的浓度,平衡体系颜色加深,D不一定是有颜色的气体 |
| C、升高温度,C百分含量减少,说明正反应是放热反应 |
| D、增大压强,平衡不移动,说明B、D是气体 |
已知下面三个数据:7.2×10-4、4.6×10-4、4.9×10-10分别是下列有关的三种酸的电离常数,若已知下列反应可以发生:NaCN+HNO2═HCN+NaNO2 NaCN+HF═HCN+NaF NaNO2+HF═HNO2+NaF.由此可判断下列叙述中不正确的是( )
| A、K(HF)=7.2×10-4 |
| B、K(HNO2)=4.9×10-10 |
| C、根据两个反应即可得出一元弱酸的强弱顺序为HF>HNO2>HCN |
| D、K(HCN)<K(HNO2)<K(HF) |
 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq) 某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下列说法正确的是( )
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq) 某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下列说法正确的是( )| A、反应I2(aq)+I-(aq)?I3-(aq)的△H>0 |
| B、若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1<K2 |
| C、若反应进行到状态D时,平衡向逆反应方向移动 |
| D、状态B与状态C相比,状态C的c(I2)大 |
 某实验小组在研究“反应条件对化学平衡的影响”时做了如下3个实验.
某实验小组在研究“反应条件对化学平衡的影响”时做了如下3个实验.