题目内容
 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq) 某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下列说法正确的是( )
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq) 某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下列说法正确的是( )| A、反应I2(aq)+I-(aq)?I3-(aq)的△H>0 |
| B、若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1<K2 |
| C、若反应进行到状态D时,平衡向逆反应方向移动 |
| D、状态B与状态C相比,状态C的c(I2)大 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:A、根据温度升高时平衡移动的方向判断反应的反应热;
B、根据温度变化时平衡移动的方向比较平衡常数的大小;
C、根据D状态与平衡状态比较,判断反应方向进而得出反应速率关系;
D、根据平衡移动规律比较浓度大小.
B、根据温度变化时平衡移动的方向比较平衡常数的大小;
C、根据D状态与平衡状态比较,判断反应方向进而得出反应速率关系;
D、根据平衡移动规律比较浓度大小.
解答:
解:A、随着温度的不断升高,I3-的浓度逐渐的减小,说明反应向逆方向移动,I2(aq)+I-(aq?I3-(aq) 是一个放热反应,即△H<0,故A错误;
B、因为K
,T2>T1,所以当温度升高时,反应向逆方向移动,即K1>K2,故B错误;
C、从图中可以看出D点并没有达到平衡状态,所以它要向A点移动,I3-的浓度应增加,平衡向正向移动,故C错误;
D、温度升高,平衡向逆方向移动,c(I3-)变小,则c(I2)应变大,所以状态B的c(I2)大,故D正确;
故选D.
B、因为K
| [I3-] |
| [I2]?[I-] |
C、从图中可以看出D点并没有达到平衡状态,所以它要向A点移动,I3-的浓度应增加,平衡向正向移动,故C错误;
D、温度升高,平衡向逆方向移动,c(I3-)变小,则c(I2)应变大,所以状态B的c(I2)大,故D正确;
故选D.
点评:本题考查化学平衡的移动和平衡常数的运用,注意化学平衡图象分析的一般方法来解答:一看面:看清图象中横坐标和纵坐标的含义;二看线:弄清图象中线的斜率或线走势的意义;三看点:明确曲线的起点、终点、交点及拐点等;四看是否需要辅助线.

练习册系列答案
相关题目
将气体A2和B2各1mol注入容积为1L的密闭容器中反应生成C,平衡时测得c(A2)=0.58mol/L,则c(B2)=0.16mol/L,c(C)=0.84mol/L,则C的分子式为( )
| A、AB2 |
| B、A2B4 |
| C、AB |
| D、A2B |
已知图一表示的是可逆反应CO(g)+H2(g)?C(s)+H2O(g)△H>0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g)?N2O4(g)△H<0的浓度(c)随时间(t)的变化情况.下列说法中正确的是( )
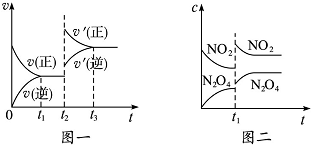

| A、图一t2时改变的条件可能是升高了温度或增大了压强 |
| B、图一t2时改变的条件一定是增大了反应物的浓度 |
| C、图二t1时改变的条件可能是升高了温度或增大了压强 |
| D、若图二t1时改变的条件是增大压强,则混合气体的平均相对分子质量将减小 |
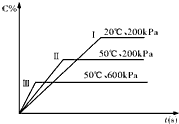 在密闭容器中进行以下可逆反应:A(g)+B(g)?C(g)+2D(?),在不同的条件下C的百分含量的变化情况如如图,则该反应描述正确的是( )
在密闭容器中进行以下可逆反应:A(g)+B(g)?C(g)+2D(?),在不同的条件下C的百分含量的变化情况如如图,则该反应描述正确的是( )| A、正反应放热,D是固体 |
| B、正反应放热,D是气体 |
| C、正反应吸热,D是气体 |
| D、正反应放热,D是固体或气体 |
可逆反应A(g)+B?C(g)+D,达到平衡时,下列说法不正确的是( )
| A、若B是气体,增大A的浓度会使B转化率增大 |
| B、若增大A的浓度,平衡体系颜色加深,D不一定是有颜色的气体 |
| C、升高温度,C百分含量减少,说明正反应是放热反应 |
| D、增大压强,平衡不移动,说明B、D是气体 |
将5.6g铁粉放入一定量某浓度的硝酸溶液中,待铁粉全部溶解后,共收集到NO、NO2(其他气体忽略不计)混合气体0.15mol,该混合气体中NO与NO2的体积比可能是( )
| A、1:2 | B、2:1 |
| C、3:2 | D、3:1 |
下列有关实验的叙述正确的是( )
| A、重结晶提纯KNO3产品除去NaCl时,应在较高温度下溶解产品配成浓溶液后冷却结晶 |
| B、用移液管移取溶液后放入锥形瓶中时,移液管下端不能接触到瓶壁 |
| C、拆卸加热装置、并有导管伸入液体中的,应先停止加热,再将导管取出液面 |
| D、用排水法收集气体时,应将导管伸入集气瓶底部 |
下列说法中正确的是( )
| A、从1 L 1 mol/L的NaCl溶液中取出100 mL,其浓度为0.1 mol/L |
| B、配制0.5 L 10 mol/L的盐酸,需要氯化氢气体112 L |
| C、0.5 L 2 mol/L BaCl2溶液中,Ba2+和Cl-总数为3×6.02×1023 |
| D、10 g 98%的硫酸(密度为1.84 g/cm3)与10 mL 18.4 mol/L硫酸的浓度是不同的 |