题目内容
已知下面三个数据:7.2×10-4、4.6×10-4、4.9×10-10分别是下列有关的三种酸的电离常数,若已知下列反应可以发生:NaCN+HNO2═HCN+NaNO2 NaCN+HF═HCN+NaF NaNO2+HF═HNO2+NaF.由此可判断下列叙述中不正确的是( )
| A、K(HF)=7.2×10-4 |
| B、K(HNO2)=4.9×10-10 |
| C、根据两个反应即可得出一元弱酸的强弱顺序为HF>HNO2>HCN |
| D、K(HCN)<K(HNO2)<K(HF) |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:相同温度下,酸的电离常数越大,该酸的酸性越强,结合强酸制取弱酸分析解答.
解答:
解:根据强酸制取弱酸知,这三种酸的酸性强弱顺序是HCN<HNO2<HF,
A.相同温度下,酸的酸性越强,其酸的电离平衡常数越大,氢氟酸的酸性最强,则氢氟酸的电离平衡常数最大,故A正确;
B.亚硝酸的酸性大于氢氰酸而小于氢氟酸,所以亚硝酸的电离平衡常数为4.6×10-4,故B错误;
C.强酸制取弱酸知,这三种酸的酸性强弱顺序是HCN<HNO2<HF,故C正确;
D.根据强酸制取弱酸知,这三种酸的酸性强弱顺序是HCN<HNO2<HF,相同温度下,酸的酸性越强,其酸的电离平衡常数越大,所以其电离平衡常数大小顺序是K(HCN)<K(HNO2)<K(HF),故D正确;
故选:B.
A.相同温度下,酸的酸性越强,其酸的电离平衡常数越大,氢氟酸的酸性最强,则氢氟酸的电离平衡常数最大,故A正确;
B.亚硝酸的酸性大于氢氰酸而小于氢氟酸,所以亚硝酸的电离平衡常数为4.6×10-4,故B错误;
C.强酸制取弱酸知,这三种酸的酸性强弱顺序是HCN<HNO2<HF,故C正确;
D.根据强酸制取弱酸知,这三种酸的酸性强弱顺序是HCN<HNO2<HF,相同温度下,酸的酸性越强,其酸的电离平衡常数越大,所以其电离平衡常数大小顺序是K(HCN)<K(HNO2)<K(HF),故D正确;
故选:B.
点评:本题考查了弱电解质的电离,明确弱酸酸性强弱与电离平衡常数的关系是解本题关键,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列实验操作或做法正确的是( )
| A、用托盘天平称量5.85 g氯化钠固体 |
| B、从试剂瓶中取Na2CO3溶液,发现取量过多,为了不浪费,把过量的试剂倒入原试剂瓶中 |
| C、用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中 |
| D、用蒸发的方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液全部加热蒸干 |
 可逆反应mX(g)+nY(g)?pZ(g),在不同的温度(T1、T2)和不同的压强(P1、P2)下,产物Z的物质的量(n)与时间(t)的关系如图所示,则下列判断正确的是( )
可逆反应mX(g)+nY(g)?pZ(g),在不同的温度(T1、T2)和不同的压强(P1、P2)下,产物Z的物质的量(n)与时间(t)的关系如图所示,则下列判断正确的是( )| A、m+n<p |
| B、m+n>p |
| C、增大压强平衡向正反应方向移动 |
| D、升高温度平衡向正反应方向移动 |
下列说法中正确的是( )
| A、平衡常数的大小与起始浓度有关 |
| B、K值越大,反应物的转化率越小 |
| C、K值越大,反应物的转化率越大 |
| D、温度越高,K值越大 |
欲使醋酸溶液中的CH3COO-浓度增大,电离平衡向右移动,且不放出气体,可向醋酸溶液中加入少量固体( )
| A、NaOH |
| B、NaHCO3 |
| C、CH3COOK |
| D、Mg |
在O.1mol/L的CH3COOH溶液中存在如下电离平衡:CH3COOH≒CH3COO-+H+对于该平衡,下列叙述正确的是
( )
( )
| A、加入少量CH3COONa固体,平衡向正反应方向移动 |
| B、加水,反应速率变小,平衡向正反应方向移动 |
| C、滴加少量0.1mol/LHCl溶液,溶液中C(H+)减少 |
| D、加入少量NaOH固体,平衡向逆反应方向移动 |
在含有NaI、Na2SO3和FeBr2 各1mol的溶液中通入足量的Cl2,将溶液在空气中加热蒸干并充分灼烧,最终得到剩余的固体物质是( )
| A、NaCl、FeCl3、Na2SO4 |
| B、NaCl、FeBr3 |
| C、NaCl、Fe2O3、Na2SO4 |
| D、Na2SO4 |
下列离子方程式书写正确的是( )
| A、Na与H2O反应:Na+H2O=Na++OH-+H2↑ | ||
| B、NH4HCO3溶液与少量NaOH溶液混合:HCO3-+OH-=CO32-+H2O | ||
| C、用小苏打治疗胃酸过多:CO32-+2H+=CO2↑+H2O | ||
D、溴代乙酸与足量氢氧化钠溶液反应:CH2BrCOOH+NaOH
|
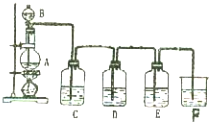 实验室用图所示装置制备氯气,并进行氯气性质实验,请回答下列问题:
实验室用图所示装置制备氯气,并进行氯气性质实验,请回答下列问题: