题目内容
 某实验小组在研究“反应条件对化学平衡的影响”时做了如下3个实验.
某实验小组在研究“反应条件对化学平衡的影响”时做了如下3个实验.(1)在氯化钴溶液中,四氯合钴(Ⅱ)离子与六水合钴(Ⅱ)离子间存在如下平衡:
[CoCl4]2-+6H2O?[Co(H2O)6]2++4Cl-
(蓝色) (粉红色)
若要将溶液变为蓝色,可采取的措施为
(2)该实验小组做乙酸乙酯的水解实验:取三支,分别注入4mL蒸馏水、4mL2mol?L-1H2SO4溶液、4mL4mol?L-1NaOH溶液,在三支试管中各加入2mL乙酸乙酯,振荡后将三支试管同时插入热水浴中,加热约5分钟,得到如图1所示的实验现象.该组同学忘记给试管编号,请分析:试管
(3)在NO2气体中存在如下平衡:2NO2(g)?N2O4(g)
(红棕色) (无色)
如图2用一支50mL注射器从储气袋中抽取30mL红棕色NO2气体,封住注射孔.当用力推压活塞,压缩注射器中的气体时,请仔细描述观察到的现象
考点:化学平衡的影响因素,油脂的性质、组成与结构
专题:化学平衡专题
分析:(1)溶液变蓝,平衡逆向移动,溶液变红,平衡正向移动,据影响平衡移动的因素分析;
(2)酸、碱对乙酸乙酯的水解具有催化作用,碱的催化作用更好,据此分析;
(3)推压活塞时,气体压强增大,平衡向正向移动,二氧化氮浓度减小,但比原平衡大.
(2)酸、碱对乙酸乙酯的水解具有催化作用,碱的催化作用更好,据此分析;
(3)推压活塞时,气体压强增大,平衡向正向移动,二氧化氮浓度减小,但比原平衡大.
解答:
解:(1)[CoCl4]2-+6H2O?[Co(H2O)6]2++4Cl-
(蓝色) (粉红色)
使溶液变蓝,可以增大氯离子浓度,使平衡逆向移动,使溶液变红,可以加入硝酸银反应掉氯离子,使平衡正向移动,故答案为:通入HCl;加入硝酸银;
(2))酸、碱对乙酸乙酯的水解具有催化作用,碱的催化作用更好,所以剩余乙酸乙酯最少的为加入碱溶液的试管,剩余乙酸乙酯最多的为加水的试管,试管A加了酸溶液,试管B加了碱溶液,试管C加了水,故答案为:B;A;
(3)推压活塞时,二氧化氮气体浓度增大,颜色变深,但气体压强增大,平衡向正向移动,二氧化氮浓度减小,但比原平衡大,所以气体颜色先变深后变浅,但比原平衡深,故答案为:气体颜色先变深后变浅;再次达到平衡.
(蓝色) (粉红色)
使溶液变蓝,可以增大氯离子浓度,使平衡逆向移动,使溶液变红,可以加入硝酸银反应掉氯离子,使平衡正向移动,故答案为:通入HCl;加入硝酸银;
(2))酸、碱对乙酸乙酯的水解具有催化作用,碱的催化作用更好,所以剩余乙酸乙酯最少的为加入碱溶液的试管,剩余乙酸乙酯最多的为加水的试管,试管A加了酸溶液,试管B加了碱溶液,试管C加了水,故答案为:B;A;
(3)推压活塞时,二氧化氮气体浓度增大,颜色变深,但气体压强增大,平衡向正向移动,二氧化氮浓度减小,但比原平衡大,所以气体颜色先变深后变浅,但比原平衡深,故答案为:气体颜色先变深后变浅;再次达到平衡.
点评:本题考查了平衡移动、乙酸乙酯的水解,题目难度中等.

练习册系列答案
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
 已知常温时CH3COOH的电离平衡常数为Ka.该温度下向20mL 0.1mol?L-1CH3COOH溶液中逐滴加入0.1mol?L-1 NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中不正确的是( )
已知常温时CH3COOH的电离平衡常数为Ka.该温度下向20mL 0.1mol?L-1CH3COOH溶液中逐滴加入0.1mol?L-1 NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中不正确的是( )| A、a点表示的溶液中c(CH3COO-)+c(OH-)=10-3mol?L-1 | ||
| B、b点所示的溶液中c(CH3COO-)+c(OH-)>(CH3COOH)+c(H+) | ||
| C、c点的含义为:CH3COOH和NaOH恰好反应完全 | ||
D、a、b、c、d点表示的溶液中
|
下列叙述正确的是( )
| A、将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO42-)=c(NH4+) |
| B、两种醋酸溶液的物质的量浓度分别c1和c2,pH分别为a和a+1,则c1<10c2 |
| C、室温下,pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,溶液呈酸性 |
D、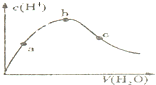 向冰醋酸中逐渐加水,有如图变化.a、b、c三点中水的电离程度最大的是b点 |
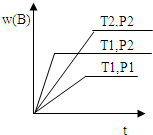 已知某反应aA(g)+bB(g)?cC(g)△H=Q 在密闭容器中进行,在不同温度(T1和T2 )及压强(P1 和P2 )下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示,下列判断正确的是( )
已知某反应aA(g)+bB(g)?cC(g)△H=Q 在密闭容器中进行,在不同温度(T1和T2 )及压强(P1 和P2 )下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示,下列判断正确的是( )| A、T1<T2,P1<P2,a+b>c,Q>0 |
| B、T1>T2,P1<P2,a+b<c,Q<0 |
| C、T1<T2,P1>P2,a+b<c,Q>0 |
| D、T1<T2,P1>P2,a+b>c,Q<0 |
在2SO2+O2=2SO3(正反应放热)的平衡体系中,下列条件可使反应速率加快,且平衡向右移动的是( )
| A、升高温度 |
| B、增加压强 |
| C、减小SO3的浓度 |
| D、使用催化剂 |
在2L密闭容器中加入或通入一定量A、B、C三种物质,在一定条件下发生反应(如图1),3min后给体系加热,气体C的体积分数Ψ(C)和混合气体的平均相对分子质量M均随温度分别发生了图示变化(如图2、图3).下列有关说法不正确的是( )
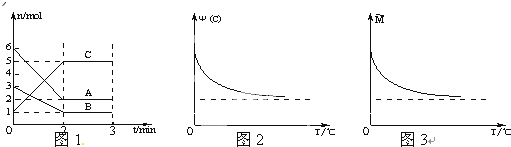

| A、前2min中C的平均反应速率为1mol/L?min |
| B、该反应的化学方程式为:2A+B?2C |
| C、正反应是放热反应 |
| D、A、B一定均为气态 |
已知:H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ?mol-1.现将一定量的稀盐酸、浓硫酸、稀醋酸分别和1L 1mol?L-1的NaOH溶液恰好完全反应,其反应热分别为△H1、△H2、△H3,则△H1、△H2和△H3的大小关系为( )
| A、△H1=△H2>△H3 |
| B、△H3>△H2>△H1 |
| C、△H2>△H1>△H3 |
| D、△H3>△H1>△H2 |
汽车尾气(含烃类、CO、NO与SO2等)是城市主要污染源之一,治理的办法之一是在汽车排气管上装催化转化器,它使NO与CO反应生成可参与大气生态循环的无毒气体,其反应原理是:2NO(g)+2CO(g)═N2(g)+2CO2(g),在298K、101kPa下△H=-113kJ?mol-1,△S=-145J?mol-1?K-1.下列说法中不正确的是( )
| A、该反应中反应物总能量高于生成物的总能量 |
| B、该反应只能在较高温度下才能自发进行 |
| C、该反应在较低温度下能自发进行,高温和催化剂条件只是加快反应的速率 |
| D、汽车尾气中的这两种气体会与人体血红蛋白结合而使人中毒 |
NA表示阿伏加德罗常数,下列说法正确的是( )
| A、16g CH4与18g NH4+所含质子数相等 |
| B、1mol 苯分子中含有碳碳双键数为3N |
| C、将分子总数为NA的NH3和HCl的混合气体置于标准状况下,其体积为约22.4L |
| D、等物质的量的甲基(-CH3)和羟基(-OH)所含电子数相等 |