在恒温时,一固定容积的容器内发生如下反应:2NO2(g)?N2O4(g) 达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数( )
| A、不变 | B、增大 |
| C、减小 | D、无法判断 |
相同物质的量的镁和铝分别与足量的稀盐酸反应,生成氢气的质量之比为( )
| A、1:1 | B、2:3 |
| C、3:4 | D、2:1 |
一定条件下将0.1mol N2和0.3mol H2置于密闭容器中发生反应N2+3H2
2NH3.下列关于该反应的说法正确的是( )
| 高温高压 |
| 催化剂 |
| A、最终可生成0.2mol NH3 |
| B、使用催化剂不影响反应速率 |
| C、升高温度反应速率增大 |
| D、增大压强反应速率减小 |
室温下,等体积的、pH=2的 HCl和CH3COOH溶液,以下说法正确的是( )
| A、两溶液中由水电离的c(H+)前者小于后者 |
| B、两溶液分别和足量的锌反应,生成氢气的体积相等 |
| C、两溶液分别和相同的锌反应,生成氢气的起始速率相等 |
| D、两溶液分别和与其体积相等的、pH=12的NaOH溶液混合后,都呈中性 |
温度为T时,向V L的密闭容器中充入一定量的A和B,发生反应:A(g)+B(g)?C(s)+xD(g)△H>0,容器中A、B、D的物质的量浓度随时间的变化如表所示.下列说法正确的是( )
| 时间 | 起始 | 5min | 10min | 15min | 20min | 25min | 30min |
| A浓度(mol?L-1) | 3.5 | 2.3 | 2.0 | 2.0 | 2.8 | 3.0 | 3.0 |
| B浓度(mol?L-1) | 2.5 | 1.3 | 1.0 | 1.0 | 1.8 | 2.0 | 2.0 |
| D浓度(mol?L-1) | 0 | 2.4 | 3.0 | 3.0 | 1.4 | 1.0 | 1.0 |
| A、反应在前10min的平均反应速率v(D)=0.3mol?L-1?min-1 | ||
B、该反应的平衡常数表达式K=
| ||
| C、若平衡时保持温度不变,压缩容器体积平衡不移动 | ||
| D、反应至15min时,改变的条件可以是升高温度 |
某温度下,已知反应mX(g)+nY(g)?qZ(g)△H>0,m+n>q,在体积一定的密闭容器中投入反应物达到平衡,下列叙述正确的是( )
| A、通惰性气体增大压强,平衡正向移动 | ||
| B、再加入X,反应吸收的热量增大 | ||
| C、增加Y的物质的量,X的转化率减小 | ||
D、降低温度,
|
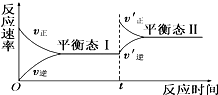 如图是恒温下化学反应“A(g)+B(g)?C(g)”的反应速率随反应时间变化的示意图,下列叙述与示意图符合的是( )
如图是恒温下化学反应“A(g)+B(g)?C(g)”的反应速率随反应时间变化的示意图,下列叙述与示意图符合的是( )| A、平衡态Ⅰ与平衡态Ⅱ的正反应速率相等 |
| B、平衡移动的原因可能是增大了反应物浓度 |
| C、平衡移动的原因可能是增大了压强 |
| D、平衡状态Ⅰ和平衡状态Ⅱ的平衡常数的大小关系为K1<K2 |
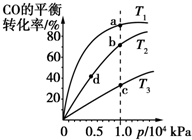 用CO合成甲醇(CH3OH)的化学反应方程式为CO(g)+2H2(g)?CH3OH(g)△H<0.按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是( )
用CO合成甲醇(CH3OH)的化学反应方程式为CO(g)+2H2(g)?CH3OH(g)△H<0.按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是( )| A、正反应速率:v(a)>v(c) v(b)>v(d) | ||||||||
| B、平衡时a点一定有n(CO):n(H2)=1:2 | ||||||||
| C、平衡常数:K(a)>K(c) K(b)=K(d) | ||||||||
D、平均摩尔质量:
|
某溶液中可能含有下列5种离子中的某几种:Na+、NH4+、Mg2+、Al3+、Clˉ.为确认该溶液组成进行如下实验:①取20.0mL该溶液,加入25.0mL 4.00mol?L-1NaOH溶液,有白色沉淀生成,但无剌激气味气体产生.过滤、洗涤、干燥,得沉淀1.16g.再将滤液稀释至100mL,测得滤液中c(OHˉ)为0.20mol?L-1;
②另取20.0mL该溶液,加入足量的AgNO3溶液,生成白色沉淀11.48g.由此可得出关于原溶液组成的正确结论是( )
②另取20.0mL该溶液,加入足量的AgNO3溶液,生成白色沉淀11.48g.由此可得出关于原溶液组成的正确结论是( )
| A、一定含有Mg2+、Al3+、Clˉ,不含Na+、NH4+ |
| B、一定含有Na+、Mg2+、Clˉ,不含NH4+,可能含有Al3+ |
| C、c (Clˉ) 为 4.00 mol?L-1,c (Al3+) 为1.00 mol?L-1 |
| D、c (Mg2+) 为 1.00 mol?L-1,c(Na+ ) 为 0.50 mol?L-1 |