题目内容
相同物质的量的镁和铝分别与足量的稀盐酸反应,生成氢气的质量之比为( )
| A、1:1 | B、2:3 |
| C、3:4 | D、2:1 |
考点:化学方程式的有关计算
专题:计算题
分析:设物质的量都为1mol,因酸足量,则金属都完全反应,然后利用化学反应方程式来计算氢气的物质的量,物质的量之比等于质量之比.
解答:
解:设金属都为1mol,Mg与足量酸反应生成氢气的物质的量为x,Al与足量酸反应生成的氢气的物质的量为y,
则Mg+2HCl═MgCl2+H2↑
1 1
1mol x
x=
=1mol,
2Al+6HCl═2AlCl3+3H2↑
2 3
1mol y
y=
=1.5mol,
物质的量之比为1mol:1.5mol=2:3,物质的量之比等于质量之比,
故选B.
则Mg+2HCl═MgCl2+H2↑
1 1
1mol x
x=
| 1×1mol |
| 1 |
2Al+6HCl═2AlCl3+3H2↑
2 3
1mol y
y=
| 1mol×3 |
| 2 |
物质的量之比为1mol:1.5mol=2:3,物质的量之比等于质量之比,
故选B.
点评:本题考查学生利用化学反应方程式的简单计算,明确酸足量,则金属完全反应是解答的关键,解答本题还可以应用关系式法、电子守恒等方法来快速解答.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列性质的比较正确的是( )
| A、酸性:H2SiO3>H2CO3 |
| B、碱性:Mg(OH)2>Al(OH)3 |
| C、稳定性:SiH4>PH3 |
| D、原子半径:N>C |
用水稀释0.1mol/L氨水时,溶液中随水量的增加而增大的是( )
| A、c(H+)和c(OH-)的乘积 | ||||
B、
| ||||
C、
| ||||
| D、pH值 |
某温度下,已知反应mX(g)+nY(g)?qZ(g)△H>0,m+n>q,在体积一定的密闭容器中投入反应物达到平衡,下列叙述正确的是( )
| A、通惰性气体增大压强,平衡正向移动 | ||
| B、再加入X,反应吸收的热量增大 | ||
| C、增加Y的物质的量,X的转化率减小 | ||
D、降低温度,
|
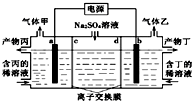 电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法正确的是( )
电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法正确的是( )| A、a极与电源的负极相连 |
| B、产物丙为硫酸溶液 |
| C、离子交换膜d为阳离子交换膜(允许阳离子通过) |
| D、a电极反应式为2H2O+2e-═2OH-+H2↑ |
 如图是学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容,据此,回答问题:
如图是学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容,据此,回答问题: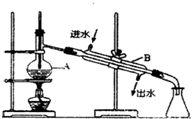 我校高一某化学兴趣小组设计了右图装置用日常生活中的饮用水制取蒸馏水的示意图,请回答下列问题.
我校高一某化学兴趣小组设计了右图装置用日常生活中的饮用水制取蒸馏水的示意图,请回答下列问题.