题目内容
温度为T时,向V L的密闭容器中充入一定量的A和B,发生反应:A(g)+B(g)?C(s)+xD(g)△H>0,容器中A、B、D的物质的量浓度随时间的变化如表所示.下列说法正确的是( )
| 时间 | 起始 | 5min | 10min | 15min | 20min | 25min | 30min |
| A浓度(mol?L-1) | 3.5 | 2.3 | 2.0 | 2.0 | 2.8 | 3.0 | 3.0 |
| B浓度(mol?L-1) | 2.5 | 1.3 | 1.0 | 1.0 | 1.8 | 2.0 | 2.0 |
| D浓度(mol?L-1) | 0 | 2.4 | 3.0 | 3.0 | 1.4 | 1.0 | 1.0 |
| A、反应在前10min的平均反应速率v(D)=0.3mol?L-1?min-1 | ||
B、该反应的平衡常数表达式K=
| ||
| C、若平衡时保持温度不变,压缩容器体积平衡不移动 | ||
| D、反应至15min时,改变的条件可以是升高温度 |
考点:化学平衡的影响因素,化学平衡建立的过程
专题:化学平衡专题
分析:A、根据v=
计算反应速率,并作判断;
B、平衡常数等于生成物浓度系数次幂之积除以反应物浓度系数次幂之积,据此写出表达式;
C、根据0到5min之间A、D的浓度变化量之比可知,D的浓度的变化量是A的2倍,A、D的浓度变化量之比等于计量数之比,所以x=2,所以该反应为气体体积不变的反应,所以压缩容器体积,平衡不移动;
D、比较15min-20min之间各物质的浓度变化量可以看出,D减小了1.6mol/L,同时A、D都增加了0.8mol/L,平衡向逆反应方向移动,因为该反应为吸热反应,所以改变的条件为降低温度,据此判断.
| △c |
| △t |
B、平衡常数等于生成物浓度系数次幂之积除以反应物浓度系数次幂之积,据此写出表达式;
C、根据0到5min之间A、D的浓度变化量之比可知,D的浓度的变化量是A的2倍,A、D的浓度变化量之比等于计量数之比,所以x=2,所以该反应为气体体积不变的反应,所以压缩容器体积,平衡不移动;
D、比较15min-20min之间各物质的浓度变化量可以看出,D减小了1.6mol/L,同时A、D都增加了0.8mol/L,平衡向逆反应方向移动,因为该反应为吸热反应,所以改变的条件为降低温度,据此判断.
解答:
解:A、根据v=
计算反应速率v(D)=
mol?L-1?min-1=0.3mol?L-1?min-1,故A正确;
B、平衡常数等于生成物浓度系数次幂之积除以反应物浓度系数次幂之积,所以反应的平衡常数表达式为K=
,C是固体,浓度可以看作是1,故B错误;
C、根据0到5min之间A、D的浓度变化量之比可知,D的浓度的变化量是A的2倍,A、D的浓度变化量之比等于计量数之比,所以x=2,所以该反应为气体体积不变的反应,所以压缩容器体积,平衡不移动,故C正确;
D、比较15min-20min之间各物质的浓度变化量可以看出,D减小了1.6mol/L,同时A、D都增加了0.8mol/L,平衡向逆反应方向移动,因为该反应为吸热反应,所以改变的条件为降低温度,故D错误;
故选AC.
| △c |
| △t |
| 3.0 |
| 10 |
B、平衡常数等于生成物浓度系数次幂之积除以反应物浓度系数次幂之积,所以反应的平衡常数表达式为K=
| [D]2 |
| [A]?[B] |
C、根据0到5min之间A、D的浓度变化量之比可知,D的浓度的变化量是A的2倍,A、D的浓度变化量之比等于计量数之比,所以x=2,所以该反应为气体体积不变的反应,所以压缩容器体积,平衡不移动,故C正确;
D、比较15min-20min之间各物质的浓度变化量可以看出,D减小了1.6mol/L,同时A、D都增加了0.8mol/L,平衡向逆反应方向移动,因为该反应为吸热反应,所以改变的条件为降低温度,故D错误;
故选AC.
点评:本题主要考查了反应速率的计算、平衡常数的表达式、影响化学平衡移动的因素等知识点,难度不大,解题时注意反应中C是固体.

练习册系列答案
 全程金卷系列答案
全程金卷系列答案
相关题目
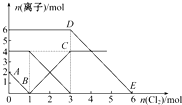 向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2═2Fe3++2Br-、2Fe3++2I-═2Fe2++I2,则下列有关说法中不正确的是( )
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2═2Fe3++2Br-、2Fe3++2I-═2Fe2++I2,则下列有关说法中不正确的是( )| A、还原性:I->Fe2+>Br- |
| B、线段AB表示Fe2+被氯气氧化 |
| C、线段BC表示生成4 mol Fe3+ |
| D、原溶液中n(Br-)=6 mol |
可以证明可逆反应N2+3H2?2NH3已达到平衡状态的是:( )
①一个N≡N键断裂的同时,有3个H-H键断裂
②其它条件不变时,混合气体平均式量不再改变
③保持其它条件不变时,体系压强不再改变
④恒温恒容时,密度保持不变
⑤NH3%不再改变
⑥2υ正(H2)=3υ逆(NH3)
⑦容器内三种气体共存
⑧N2、H2、NH3分子式之比为1:3:2.
①一个N≡N键断裂的同时,有3个H-H键断裂
②其它条件不变时,混合气体平均式量不再改变
③保持其它条件不变时,体系压强不再改变
④恒温恒容时,密度保持不变
⑤NH3%不再改变
⑥2υ正(H2)=3υ逆(NH3)
⑦容器内三种气体共存
⑧N2、H2、NH3分子式之比为1:3:2.
| A、全部 | B、只有①③⑤ |
| C、②③⑤⑥ | D、只有③⑤⑥ |
 向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:xA(g)+B(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别用下表和如图表示:下列说法正确的是( )
向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:xA(g)+B(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别用下表和如图表示:下列说法正确的是( )| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | 1.0L |
| 温度 | T1 | T2 | T2 |
| 反应物 起始量 | 0.5molA 1.5molB | 0.5molA 1.5molB | 2.0molA 6.0molB |
| A、由图可知:T1<T2,且该反应为吸热反应 |
| B、T2时该反应的平衡常数K=0.8 |
| C、前10min乙、丙两容器中v(A)乙>v(A)丙 |
| D、C的质量m:m甲=m乙<2m丙 |
在恒温时,一固定容积的容器内发生如下反应:2NO2(g)?N2O4(g) 达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数( )
| A、不变 | B、增大 |
| C、减小 | D、无法判断 |
下列实验操作正确的是( )
| A、将氢氧化钠固体放在滤纸上称量 |
| B、用10 mL量筒量取8.58 mL蒸馏水 |
| C、硅酸钠溶液保存在橡胶塞的试剂瓶中 |
| D、用广泛pH试纸测定某浓度醋酸溶液的pH为4.5 |
2013年下半年,武汉雾霾天气特别多,空气污染严重.湖北省决定在“十二五”期间,将大力实施“清水蓝天”工程.不利于“清水蓝天”工程实施的是( )
| A、加强城市生活污水脱氮除磷处理,遏制水体富营养化 |
| B、为防止电池中的重金属污染,废旧电池应作深埋处理 |
| C、积极推广太阳能、风能、地热能及水能等的使用,减少化石燃料的使用 |
| D、大力实施矿物燃料“脱硫、脱硝技术”,减少硫的氧化物和氮的氧化物污染 |