在恒温下的密闭容器中,有可逆反应:2NO+O2?2NO2 (正反应为放热反应),不能说明已经达到平衡状态的是( )
| A、正反应生成 NO2 的速率和逆反应生成 O2 的速率相等 |
| B、反应容器中压强不随时间的变化而变化 |
| C、混合气体颜色深浅保持不变 |
| D、混合气体的平均相对分子质量不随时间变化而变化 |
下列关于电解质的说法正确的是( )
| A、NaOH溶液能导电,所以NaOH溶液为电解质 |
| B、氯化钠晶体不能导电,所以氯化钠为非电解质 |
| C、虽然液态氯化氢不导电,但氯化氢属于电解质 |
| D、液态的铜导电性很好,所以铜是电解质 |
下列叙述正确的是( )
| A、电解质的电离是在通电的条件下进行的 |
| B、强电解质溶液的导电能力不一定比弱电解质溶液强 |
| C、盐酸是强电解质,所以盐酸中没有HCl分子 |
| D、H2O(g)═H2O(l)是放热反应 |
在0.1mol?L-1 CH3COOH溶液中存在如下电离平衡:CH3COOH═CH3COO-+H+,对于该平衡,下列叙述正确的是( )
| A、加入水时,平衡向逆反应方向移动 |
| B、加入少量NaOH固体,平衡向正反应方向移动 |
| C、加入少量0.1mol?L-1HCl溶液,溶液中C(H+)增大 |
| D、加入少量CH3COONa固体,平衡向正反应方向移动 |
化学在生产和日常生活中有着重要的应用.下列叙述正确的是( )
| A、盐酸滴定氨水,可以选择酚酞为指示剂 |
| B、电离程度(同温度同浓度溶液中):HCl>CH3OOH>NaHCO3 |
| C、分散质粒子的直径:FeCl3溶液>Fe(OH)3胶体>Fe(OH)3悬浊液 |
| D、若要使Na2S溶液中c(Na+)/c(S2-)的值减小,可以加入适量的KOH固体 |
下列有关化学用语使用正确的是( )
A、硫原子的原子结构示意图: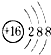 | ||
B、NH4Cl的电子式: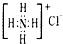 | ||
C、核内有8个中子的碳原子:
| ||
| D、HCO3-电离的离子方程式:HCO3-+H2O?CO32-+H3O+ |
24mL浓度为0.05mol?L-1的Na2SO3溶液,恰好与20mL浓度为0.02mol?L-1的K2Cr2O7溶液完全反应,已知Na2SO3能被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为( )
| A、+2 | B、+3 | C、+4 | D、+5 |
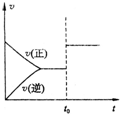 某温度下,将2mol A和3mol B充入一密闭容器中,发生反应aA(g)+B(g)?C(g)+D(g),5min后达到平衡.已知该温度下其平衡常数K=1,在t0时刻,若保持温度不变将容器体积扩大为原来的10倍,A的转化率不发生变化,则下列说法正确的是( )
某温度下,将2mol A和3mol B充入一密闭容器中,发生反应aA(g)+B(g)?C(g)+D(g),5min后达到平衡.已知该温度下其平衡常数K=1,在t0时刻,若保持温度不变将容器体积扩大为原来的10倍,A的转化率不发生变化,则下列说法正确的是( )| A、a=2 |
| B、达平衡时A的转化率为60% |
| C、速率随时间变化关系如右图所示 |
| D、为提高A的转化率,可采取升高温度的措施 |
下列有关化学用语表示正确的是( )
A、过氧化氢电子式: | ||
B、中子数为28的钙原子:
| ||
C、铝离子结构示意图: | ||
D、2,4,6-三溴苯酚: |
 已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO42-.向含3mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示.
已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO42-.向含3mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示.