题目内容
下列有关化学用语使用正确的是( )
A、硫原子的原子结构示意图: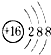 | ||
B、NH4Cl的电子式: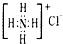 | ||
C、核内有8个中子的碳原子:
| ||
| D、HCO3-电离的离子方程式:HCO3-+H2O?CO32-+H3O+ |
考点:电子式、化学式或化学符号及名称的综合,原子结构示意图,离子方程式的书写
专题:
分析:A.硫原子最外层有6个电子, 为硫离子的结构示意图;
为硫离子的结构示意图;
B.氯离子为阴离子,电子式中氯离子应用括号及标出孤对电子;
C.质量数=质子数+中子数,元素符号的左上角表示质量数,左下角为质子数;
D.碳酸氢根离子在溶液中部分电离出氢离子和碳酸根离子,电离程度较弱.
 为硫离子的结构示意图;
为硫离子的结构示意图;B.氯离子为阴离子,电子式中氯离子应用括号及标出孤对电子;
C.质量数=质子数+中子数,元素符号的左上角表示质量数,左下角为质子数;
D.碳酸氢根离子在溶液中部分电离出氢离子和碳酸根离子,电离程度较弱.
解答:
解:解:A.硫原子最外层有6个电子,则硫原子结构示意图为 ,故A错误;
,故A错误;
B.氯离子应用括号及标出孤对电子,其电子式为 ,故B错误;
,故B错误;
C.原子核内有8个中子的C原子,质子数为6,质量数为14,则原子核内有8个中子的碳原子表示为:
C,故C错误;
D.碳酸氢根离子的电离为可逆过程,且电离程度较弱,其电离的离子方程式为:HCO3-+H2O?CO32-+H3O+,故D正确;
故选D.
 ,故A错误;
,故A错误;B.氯离子应用括号及标出孤对电子,其电子式为
 ,故B错误;
,故B错误;C.原子核内有8个中子的C原子,质子数为6,质量数为14,则原子核内有8个中子的碳原子表示为:
8 6 |
D.碳酸氢根离子的电离为可逆过程,且电离程度较弱,其电离的离子方程式为:HCO3-+H2O?CO32-+H3O+,故D正确;
故选D.
点评:本题考查化学用语的书写判断,涉及电子式、原子结构示意图、原子构成、电离方程式等知识,注重基础知识的考查,把握化学用语的规范使用,题目难度不大.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案
相关题目
下列有关实验操作、现象或实验原理的叙述,错误的是( )
| A、减压过滤不宜用于过滤胶状沉淀或颗粒太小的沉淀,沉淀的颗粒较大时,可用倾析法将固体与溶液分离 |
| B、制备阿司匹林时,将反应物置于水浴85~90℃的锥形瓶中充分反应5~10min,冷却后,向锥形瓶中加一定量的水可以促进产物的析出 |
| C、牙膏中的安息香酸钠、氟化钠溶于水,水解使溶液呈碱性,可以预防龋齿 |
| D、由Zn-Cu/稀硫酸构成的原电池溶液中加入适量的H2O2能提高电池的放电效率 |
下列各组离子中,能在溶液中大量共存的是( )
| A、Na+、Cu2+、Cl-、SO42- |
| B、H+、Cl-、CO32-、SO42- |
| C、Ba2+、Na+、SO42-、Cl- |
| D、H+、K+、OH-、Cl- |
稀氨水中存在着下列平衡:NH3?H2O?NH4++OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入适量的物质是( )
| A、NH4Cl |
| B、硫酸 |
| C、NaOH固体 |
| D、水 |
在恒温下的密闭容器中,有可逆反应:2NO+O2?2NO2 (正反应为放热反应),不能说明已经达到平衡状态的是( )
| A、正反应生成 NO2 的速率和逆反应生成 O2 的速率相等 |
| B、反应容器中压强不随时间的变化而变化 |
| C、混合气体颜色深浅保持不变 |
| D、混合气体的平均相对分子质量不随时间变化而变化 |