题目内容
下列有关化学用语表示正确的是( )
A、过氧化氢电子式: | ||
B、中子数为28的钙原子:
| ||
C、铝离子结构示意图: | ||
D、2,4,6-三溴苯酚: |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.过氧化氢是共价化合物,不存在阴阳离子;
B.元素符号的左上角表示质量数,左下角表示质子数,质量数=质子数+中子数;
C.铝离子有2个电子层,最外层电子数为8;
D.苯酚中羟基的邻位、对位氢原子被溴原子取代生成2,4,6-三溴苯酚.
B.元素符号的左上角表示质量数,左下角表示质子数,质量数=质子数+中子数;
C.铝离子有2个电子层,最外层电子数为8;
D.苯酚中羟基的邻位、对位氢原子被溴原子取代生成2,4,6-三溴苯酚.
解答:
解:A.过氧化氢是共价化合物,分子中不存在阴阳离子,过氧化氢正确的电子式为: ,故A错误;
,故A错误;
B.中子数为28的钙原子,其质量数为48,该钙原子正确的表示方法为:2048Ca,故B错误;
C.铝离子核外电子总数为10,最外层为8个电子,正确的结构示意图为 ,故C错误;
,故C错误;
D.2,4,6-三溴苯酚的结构简式为: ,故D正确;
,故D正确;
故选D.
 ,故A错误;
,故A错误;B.中子数为28的钙原子,其质量数为48,该钙原子正确的表示方法为:2048Ca,故B错误;
C.铝离子核外电子总数为10,最外层为8个电子,正确的结构示意图为
 ,故C错误;
,故C错误;D.2,4,6-三溴苯酚的结构简式为:
 ,故D正确;
,故D正确;故选D.
点评:本题考查了常见化学用语的判断,题目难度中等,注意掌握离子结构示意图、电子式、元素符号、结构简式等化学用语的概念及书写原则,试题侧重基础知识的考查,有利于培养学生灵活应用所学知识的能力.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案
相关题目
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
A、已知:
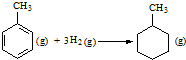 的△H为-384 kJ?mol-1 的△H为-384 kJ?mol-1 | ||||||||||
| B、将足量SO2通入Ba(NO3)2溶液中有沉淀生成的离子方程式,3SO2+Ba2++2NO3-+2H2O=BaSO4↓+2NO+2SO42-+4H+ | ||||||||||
| C、电解稀硫酸不可能发生的反应:Cu+H2SO4=CuSO4+H2↑ | ||||||||||
| D、1000℃时,Na2SO4与H2发生反应:Na2SO4(s)+4H2(g)?Na2S(s)+4H2O(g)△H>0,反应达到平衡后,将体系中的Na2S(s)全部移走,平衡不移动 |
下列物质不能通过单质直接化合制备的是( )
| A、Na2S |
| B、FeCl2 |
| C、Na2O2 |
| D、CuCl2 |
下列对于25℃时pH为12的氨水,叙述正确的是( )
| A、加入一定量pH=2的醋酸,混合后所得的溶液中:c(CH3COO-)+c(OH-)=c(NH4+)+c(H+) |
| B、向其中加入一定量的水,NH3?H2O的电离平衡正移,溶液中所有离子浓度均减小 |
| C、与等体积、pH=2的盐酸混合后所得的溶液中:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D、c(NH4+)+c(NH3?H2O)=1.0×10-12 mol?L-1 |
在0.1mol?L-1 CH3COOH溶液中存在如下电离平衡:CH3COOH═CH3COO-+H+,对于该平衡,下列叙述正确的是( )
| A、加入水时,平衡向逆反应方向移动 |
| B、加入少量NaOH固体,平衡向正反应方向移动 |
| C、加入少量0.1mol?L-1HCl溶液,溶液中C(H+)增大 |
| D、加入少量CH3COONa固体,平衡向正反应方向移动 |
从下列事实,找出不能用勒沙特列原理解释的是( )
| A、在溴水中存在如下平衡:Br2+H2O=HBr+HBrO,当加入NaOH溶液后颜色变浅 |
| B、对2HI?H2+I2(气)平衡体系增加压强使颜色变深 |
| C、反应CO+NO2?CO2+NO(△H<0)升高温度使平衡向逆方向移动 |
| D、合成氨反应:N2+3H2?2NH3(△H<0),为使氨的产率提高,理论上应采取低温高压的措施 |
与100mL 0.1mol/LNa2SO4溶液中Na+离子浓度相同的是( )
| A、10mL 1mol/L Na2SO4溶液 |
| B、50mL 0.2mol/L NaCl溶液 |
| C、10mL 0.2mol/LNa2SO4溶液 |
| D、200mL 0.1mol/L NaNO3溶液 |
工业上制备HNO3的最后一步方程式为:3NO2+H2O═2HNO3+NO,发生还原反应和氧化反应的物质的质量比为( )
| A、3:1 | B、1:3 |
| C、1:2 | D、2:1 |