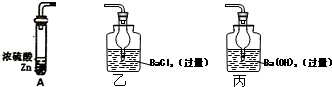设NA代表阿伏伽德罗常数的值,下列说法正确的是( )
| A、标准状况下,22.4L水所含的分子数为NA | ||||
| B、17g NH3中所含的原子个数为4NA | ||||
| C、1L、1mol/L的稀盐酸中含有的氯化氢分子数为NA | ||||
D、在反应2H2O2
|
向10mL 1.5mol/L的硫酸铝溶液加入30mL NaOH溶液,充分反应后得到1.56g沉淀,则NaOH溶液的物质的量浓度是( )
| A、1mol/L |
| B、2mol/L |
| C、5mol/L |
| D、3.3mol/L |
X、Y、M、N是短周期主族元素,且原子序数依次增大.已知X的最外层电子数是电子层数的3倍,X、M同主族,Y的原子在短周期主族元素中原子半径最大.下列说法正确的是( )
| A、M与X形成的化合物对应的水化物一定是强酸 |
| B、Y2X和Y2X2中阴、阳离子的个数比相同,化学键类型也完全相同 |
| C、X、Y的简单离子半径:r(X2-)>r(Y+) |
| D、M的气态氢化物比N的气态氢化物稳定 |
短周期的A、B、C、D、E物种元素,原子序数依次增大.已知元素A的气态氢化物和A的最高价氧化物对应的水化物反应生成盐;B、E为同主族元素,B元素原子最外层电子数是次外层的3倍;D是地壳中含量最多的金属元素;C是短周期中与水反应最激烈的金属元素.下列叙述不正确的是( )
| A、原子半径:C>D>B |
| B、元素B的气体氢化物的沸点比元素E气体氢化物的沸点高 |
| C、元素A的氧化物的大量排放能引起温室效应 |
| D、元素C、D、E的最高价氧化物对应的水化物两两之间能发生反应 |
在相同温度时,100mL0.01mol?L-1的醋酸溶液与10mL 0.1mol?L-1的醋酸溶液相比较,下列数值或性质中,前者大于或强于后者的是( )
| A、H+的物质的量 |
| B、醋酸的电离常数 |
| C、中和时所需NaOH的量 |
| D、溶液的导电性 |
在可逆反应2A(g)+3B(g)?xC(g)+D(g)中,起始浓度A为5mol?L-1,B为3mol?L-1,C的反应速率为0.5mol?(L?min)-1,2min后,测得D的浓度为0.5mol?L-1.则关于此反应的下列说法中正确的是( )
| A、2 min末时,A和B的浓度之比为5:3 |
| B、x=1 |
| C、2 min末时,B的浓度为1.5 mol?L-1 |
| D、2 min末时,A的消耗浓度为0.5 mol?L-1 |
短周期主族元素X、Y、Z、W的原子序数依次增大.X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构,W与X同主族.下列说法正确的是( )
| A、Y的气态简单氢化物的热稳定性比W的强 |
| B、X的最高价氧化物对应水化物的酸性比W的弱 |
| C、Y分别与Z、W形成的化合物均为碱性氧化物 |
| D、原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X) |