化学在生产和日常生活中有着重要的应用.下列说法正确是( )
| A、高纯度的硅单质广泛用于制作光导纤维 |
| B、向煤中加入适量石灰石,在煤燃烧时SO2最终生成CaSO3,可减少对大气的污染 |
| C、汽车的排气管上装有“催化转化器”,使有毒的CO和NO反应生成N2和CO2 |
| D、大量燃烧化石燃料排放的废气中含大量CO2、SO2造成大气污染,从而使雨水pH=5.6形成酸雨 |
工业制硝酸的其中一步反应为氨的氧化,反应方程式为:
4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-1025kJ/mol氧化过程中还伴随有N2O、N2等物质生成.有关该反应的说法正确的是( )
4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-1025kJ/mol氧化过程中还伴随有N2O、N2等物质生成.有关该反应的说法正确的是( )
| A、此反应物的总能量低于生成物的总能量 |
| B、反应达到平衡后,3ν正(NH3)=2ν逆(H2O) |
| C、其它条件不变,温度越高,氨的转化率越高 |
| D、寻找合适的催化剂是加快反应速率的有效措施 |
下列物质与水反应,能放出氧气的是( )
| A、Na |
| B、Na2O |
| C、Na2O2 |
| D、NO2 |
反应C(s)+H2O(g)?CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎没影响的是( )
| A、增加C的量 |
| B、将容器的体积缩小一半 |
| C、投入一块钠 |
| D、保持压强不变,充入Ar使容器容积变大 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、标准状况下,22.4 L H2O含有的分子数为NA |
| B、500mL1moL/L的盐酸溶液中含有的HCl分子数为0.5NA |
| C、将1L2mol/L的FeCl3溶液制成胶体后,其中含有氢氧化铁胶粒数为2NA |
| D、23gNa与O2在不同条件下反应虽分别生成Na2O和Na2O2,但转移的电子数一定为 NA |
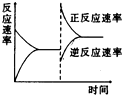 如图是改变某一外界条件后反应A2(s)+3B2(g)?2C(g)△H<0的反应速率与时间图象,则改变的条件可能是( )
如图是改变某一外界条件后反应A2(s)+3B2(g)?2C(g)△H<0的反应速率与时间图象,则改变的条件可能是( )| A、升高温度,同时加压 |
| B、保持体系压强不变加入反应物A2 |
| C、降低温度,同时减压 |
| D、保持体系压强不变加入反应物B2 |
在一定温度下,下列叙述不是可逆反应A(g)+3B(g)?2C(g)达到平衡的标志的是( )
(1)C的生成速率与C的分解速率相等;
(2)单位时间内amol A生成,同时生成3amolB;
(3)A、B、C的浓度不再变化;
(4)混合气体的总压强不再变化;
(5)混合气体的物质的量不再变化;
(6)单位时间消耗amol A,同时生成3amolB.
(1)C的生成速率与C的分解速率相等;
(2)单位时间内amol A生成,同时生成3amolB;
(3)A、B、C的浓度不再变化;
(4)混合气体的总压强不再变化;
(5)混合气体的物质的量不再变化;
(6)单位时间消耗amol A,同时生成3amolB.
| A、(2)(5) |
| B、(1)(3) |
| C、(2) |
| D、(5)(6) |
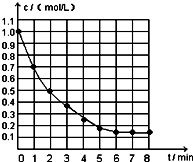 如图表示反应X(g)═4Y(g)+Z(g)△H<0,在某温度时X的浓度
如图表示反应X(g)═4Y(g)+Z(g)△H<0,在某温度时X的浓度随时间变化的曲线.下列有关该反应的描述正确的是( )
| A、该反应的过程是熵减小的过程 |
| B、若降低温度,v正减小,v逆增大 |
| C、第6min后,反应就停止了 |
| D、X在第一分钟和第二分钟内的平均反应速率之比是3:2 |
可逆反应mA(固)+nB(气)?Pc (气)+qD(气)反应过程中其他条件不变时C的百分含量C%与温度(T)和压强(p)的关系如图所示,下列叙述中正确的是( )
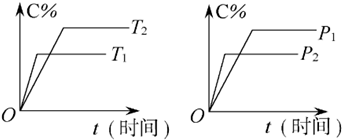

| A、达到平衡后,使用催化剂,C%将增大 |
| B、达到平衡后,若升高温度,化学平衡向逆反应方向移动 |
| C、方程式中n>p+q |
| D、达到平衡后,增加A的量有利于化学平衡向正反应方向移动 |