题目内容
化学在生产和日常生活中有着重要的应用.下列说法正确是( )
| A、高纯度的硅单质广泛用于制作光导纤维 |
| B、向煤中加入适量石灰石,在煤燃烧时SO2最终生成CaSO3,可减少对大气的污染 |
| C、汽车的排气管上装有“催化转化器”,使有毒的CO和NO反应生成N2和CO2 |
| D、大量燃烧化石燃料排放的废气中含大量CO2、SO2造成大气污染,从而使雨水pH=5.6形成酸雨 |
考点:硅和二氧化硅,二氧化硫的污染及治理,常见的生活环境的污染及治理
专题:化学应用
分析:A、单质硅是半导体,二氧化硅可以制光导纤维;
B、石灰石高温煅烧产生的氧化钙可以和二氧化硫之间反应,最终得到稳定的硫酸钙;
C、根据有毒气体的转化进行分析;
D、酸雨pH<5.6.
B、石灰石高温煅烧产生的氧化钙可以和二氧化硫之间反应,最终得到稳定的硫酸钙;
C、根据有毒气体的转化进行分析;
D、酸雨pH<5.6.
解答:
解:A、高纯度的硅单质是半导体,广泛用于制作芯片,二氧化硅可以制光导纤维,故A错误;
B、石灰石高温煅烧产生的氧化钙可以和有毒气体二氧化硫之间反应,生成亚硫酸钙不稳定,易被氧气氧化为稳定的硫酸钙,实现煤的脱硫,故B错误;
C、汽车的排气管上装有“催化转化器“,使有毒的CO和NO反应生成N2和CO2,故C正确;
D、正常雨水的pH约为5.6,酸雨pH<5.6,故D错误.
故选C.
B、石灰石高温煅烧产生的氧化钙可以和有毒气体二氧化硫之间反应,生成亚硫酸钙不稳定,易被氧气氧化为稳定的硫酸钙,实现煤的脱硫,故B错误;
C、汽车的排气管上装有“催化转化器“,使有毒的CO和NO反应生成N2和CO2,故C正确;
D、正常雨水的pH约为5.6,酸雨pH<5.6,故D错误.
故选C.
点评:本题考查学生硅、二氧化硅的用途知识以及环境污染等问题,注意二氧化硅是酸性氧化物,不溶于水,不能用二氧化硅制取硅酸,难度不大.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案
相关题目
2010年1月12日海地当地时间16时53分(北京时间1月13日5时53分),海地遭遇500年来最强地震,在抗震救灾中要用大量漂白粉和漂白液杀菌消毒.下列说法中正确的是( )
| A、漂白粉是纯净物,漂白液是混合物 |
| B、漂白粉的有效成分是Ca(ClO)2 |
| C、工业上将氯气通入澄清石灰水制取漂白粉 |
| D、漂白液的有效成分是Na2O2 |
对于密闭容器中进行的反应CO(g)+H2O(g)?CO2 (g)+H2(g),达到平衡后,其他条件不变,增大CO的浓度,下列说法不正确的是( )
| A、正反应速率增大 |
| B、逆反应速率先减小后增大 |
| C、达到平衡时,逆反应速率比原平衡要大 |
| D、CO的转化率降低 |
“酸雨”的形成主要是由于( )
| A、森林遭到乱砍伐,破坏了生态平衡 |
| B、工业上大量燃烧含硫的燃料 |
| C、大气中CO2的含量增多 |
| D、汽车排出大量尾气 |

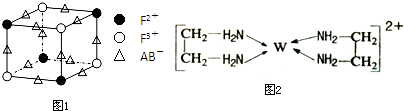 已知A、B、C、D、E、F、W都是周期表中前四周期的元素,它们的核电荷数依次增大,其中A、B、C、D、E为不同主族的元素.A、C的最外层电子数都是其电子层数的2倍,B的电负性大于C,透过蓝色钴玻璃观察E的焰色反应为紫色,F的基态原子中有4个未成对电子,W的+1价阳离子正好充满K,L,M三个电子层.回答下列问题:
已知A、B、C、D、E、F、W都是周期表中前四周期的元素,它们的核电荷数依次增大,其中A、B、C、D、E为不同主族的元素.A、C的最外层电子数都是其电子层数的2倍,B的电负性大于C,透过蓝色钴玻璃观察E的焰色反应为紫色,F的基态原子中有4个未成对电子,W的+1价阳离子正好充满K,L,M三个电子层.回答下列问题: