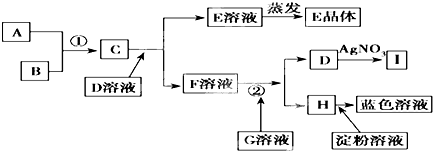
已知某溶液中仅存在OH-、H+、NH4+、Cl-四种离子,其浓度大小有如下关系,其中一定不正确的是( )
| A、C(Cl-)>C(NH4+)>C(H+)>C(OH-) |
| B、C(C1-)=C(NH4+),且C(H+)═C(OH-) |
| C、C(NH4+)<C(Cl-)<C(H+)<C(OH-) |
| D、C(OH-)<C(NH4+)<C(H+)<C(Cl-) |
R2O8n-离子在一定条件下可以把Mn2-氧化为MnO4,若反应后R2O8n-离子变为RO42离子,知反应中氧化剂与还原剂的离子数之比为5:2,则R2O8n-离子中R元素的化合价以及n值分别为( )
| A、+7、2 | B、+6、2 |
| C、+5、1 | D、+4、1 |
25℃时,二元酸H2CO3的溶液中离子种类分布如图,H2CO3、HCO3-、CO32-的浓度总和为为0.1mol?L-1,现有一组Na2CO3和NaHCO3混合溶液,下列有关溶液中离子浓度关系的叙述正确的是( )


| A、pH=11的溶液中,c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) |
| B、W点所表示的溶液中:c(Na+)=0.15mol?L-1 |
| C、pH=8.4的溶液中,c(OH-)=c(H+)+c(HCO3-)+2c(CO32-) |
| D、pH=9时,c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-) |
酸性KMnO4溶液恰好能氧化KHC2O4?H2C2O4?2H2O,等体积混合酸性KMnO4溶液和KHC2O4?H2C2O4?2H2O所配成的溶液,得到40ml混合溶液和标准状态下0.56LCO2,则原KMnO4溶液的浓度(mol?L-1)为( )
提示:①H2C2O4是二元弱酸,其中C为+2价
②10(KHC2O4?H2C2O4)+8KMnO4+17H2SO4=8MnSO4+9K2SO4+40CO2↑+32H2O
③溶液混合后忽略体积变化.
提示:①H2C2O4是二元弱酸,其中C为+2价
②10(KHC2O4?H2C2O4)+8KMnO4+17H2SO4=8MnSO4+9K2SO4+40CO2↑+32H2O
③溶液混合后忽略体积变化.
| A、0.005mol?L-1 |
| B、0.08mol?L-1 |
| C、0.125mol?L-1 |
| D、0.25mol?L-1 |
在2L密闭容器中充有2mol SO2和一定量的O2,发生反应2SO2(g)+O2(g)
2SO3(g).当反应进行到4min时,测得此时SO2为0.4mol,那么反应进行到2min时,密闭容器中SO2物质的量是( )
| 催化剂 |
| △ |
| A、1.6 mol |
| B、1.2 mol |
| C、大于1.6 mol |
| D、小于1.2 mol |
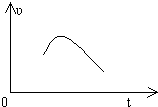 把镁条投入到盛有盐酸的敞口容器中,产生H2的速率可由如图表示,在下列因素中,①盐酸的浓度,②镁条的表面积,③溶液的温度,④氯离子的浓度,影响反应速率的因素是( )
把镁条投入到盛有盐酸的敞口容器中,产生H2的速率可由如图表示,在下列因素中,①盐酸的浓度,②镁条的表面积,③溶液的温度,④氯离子的浓度,影响反应速率的因素是( )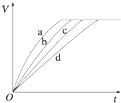 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体积V的数据,根据数据绘制得如图,则曲线a、b、c、d所对应的实验组别可能是( )
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体积V的数据,根据数据绘制得如图,则曲线a、b、c、d所对应的实验组别可能是( )