题目内容
某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率.请回答下列问题:
(1)硫酸铜溶液可以加快氢气生成速率的原因
(2)实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与上述实验中CuSO4溶液起相似作用的是 .
(3)要加快上述实验中气体产生的速率,还可采取的措施有(答两种): 、 .
(1)硫酸铜溶液可以加快氢气生成速率的原因
(2)实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与上述实验中CuSO4溶液起相似作用的是
(3)要加快上述实验中气体产生的速率,还可采取的措施有(答两种):
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:(1)Zn和硫酸的反应中加入少量的CuSO4溶液,能置换出一定量Cu,在溶液中形成Cu/Zn原电池,原电池反应比化学反应速率快;
(2)所给四种溶液中只Zn只能置换出Ag;
(3)从影响反应速率的因素分析.
(2)所给四种溶液中只Zn只能置换出Ag;
(3)从影响反应速率的因素分析.
解答:
解:(1)Zn和硫酸的反应中加入少量的CuSO4溶液,能置换出一定量Cu,在溶液中形成Cu/Zn原电池,而加快化学反应速率,
故答案为:CuSO4与Zn反应产生的Cu与Zn形成Cu-Zn原电池,加快了氢气生成的速率;
(2)所给四种溶液中只Zn只能置换出Ag,即Ag2SO4与CuSO4溶液具有相似的作用,故答案为:Ag2SO4;
(3)为加快Zn和硫酸的反应速率可从升温、适当增大硫酸的浓度、增大锌的比表面积等角度考虑,故答案为:增加锌的表面积;升高温度或适当增大硫酸的浓度等.
故答案为:CuSO4与Zn反应产生的Cu与Zn形成Cu-Zn原电池,加快了氢气生成的速率;
(2)所给四种溶液中只Zn只能置换出Ag,即Ag2SO4与CuSO4溶液具有相似的作用,故答案为:Ag2SO4;
(3)为加快Zn和硫酸的反应速率可从升温、适当增大硫酸的浓度、增大锌的比表面积等角度考虑,故答案为:增加锌的表面积;升高温度或适当增大硫酸的浓度等.
点评:本题主要考查影响化学反应速率的因素,并结合数据分析CuSO4溶液对化学反应速率的影响等.侧重考查考生运用所学知识灵活作答,根据实验分析问题的思维能力,题目难度不大.

练习册系列答案
相关题目
四种主族元素的离子aXm+、bYn+、cZn-和dRm-(a、b、c、d为元素的原子序数),它们具有相同的电子层结构,若m>n,则对下列叙述的判断正确的是( )
①a-b=m-n ②元素的原子序数a>b>c>d
③元素非金属性Z>R ④最高价氧化物对应水化物的碱性X>Y.
①a-b=m-n ②元素的原子序数a>b>c>d
③元素非金属性Z>R ④最高价氧化物对应水化物的碱性X>Y.
| A、②③ | B、③ |
| C、①②③④ | D、①②③ |
分离下列三组混合物依次采取的方法正确的是:①氯化钠溶液和鸡蛋清 ②植物油和氯化钠溶液 ③碳酸钙和氯化钙的溶液( )
| A、渗析、蒸馏、萃取 |
| B、渗析、分液、过滤 |
| C、分液、过滤、加热升华 |
| D、蒸馏、萃取、分液 |
下列各组溶液不加任何试剂,只需要用试管和滴管两两互滴就能鉴别的是( )
| A、盐酸、氢氧化钠、氯化钠 |
| B、氢氧化钠、氢氧化钡、硫酸 |
| C、硫酸氢钠、碳酸钠、氢氧化钠 |
| D、硫酸铜、盐酸、硫酸 |
可逆反应mA(气)+nB?pC(气)+qD(其中A和C都是无色气体),当达到平衡时,下列叙述正确的是( )
| A、增大压强,平衡不移动,说明(m+n)一定等于(p+q) |
| B、升高温度,A的转化率减小,说明正反应是吸热反应 |
| C、若增加B的量,平衡体系颜色加深,说明B必是气体物质 |
| D、若B是气体,增加A的量,A、B转化率都一定增大 |
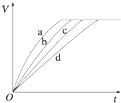 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体积V的数据,根据数据绘制得如图,则曲线a、b、c、d所对应的实验组别可能是( )
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体积V的数据,根据数据绘制得如图,则曲线a、b、c、d所对应的实验组别可能是( )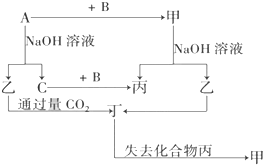 由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有如图示的转换关系,已知C为密度最小的气体,甲是电解质.
由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有如图示的转换关系,已知C为密度最小的气体,甲是电解质.