已知I-、Fe2+、SO2、Cl-和H2O2均有还原性、它们在酸性溶液中还原性强弱顺序为Cl-<H2O2<Fe2+<I-<SO2,则下列反应不能发生的是( )
| A、2Fe2++I2=2Fe3++2I- |
| B、2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ |
| C、SO2+I2+2H2O=H2SO4+2HI |
| D、H2O2+SO2=H2SO4 |
根据下列化学方程式,判断有关物质的还原性强弱的顺序为( )
①I2+SO2+2H2O═H2SO4+2HI;
②2FeCl2+Cl2═2FeCl3;
③2FeCl3+2HI═2FeCl2+2HCl+I2.
①I2+SO2+2H2O═H2SO4+2HI;
②2FeCl2+Cl2═2FeCl3;
③2FeCl3+2HI═2FeCl2+2HCl+I2.
| A、I->Fe2+>Cl->SO2 |
| B、Cl->Fe2+>SO2>I- |
| C、Fe2+>I->Cl->SO2 |
| D、SO2>I->Fe2+>Cl- |
 二茂铁[(C5H5)2Fe]分子是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等.它的结构如下图所示,下列说法正确的是( )
二茂铁[(C5H5)2Fe]分子是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等.它的结构如下图所示,下列说法正确的是( )| A、二茂铁中Fe2+与环戊二烯离子(C5H5-)之间为离子键 |
B、1mol环戊二烯(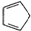 )中含有σ键的数目为5NA )中含有σ键的数目为5NA |
| C、分子中存在π键 |
| D、Fe2+的电子排布式为1s22s22p63s23p63d44s2 |
下列变化过程,属于放热过程的是( )
①液态水变成水蒸气
②酸碱中和反应
③浓H2SO4稀释
④固体氢氧化钠溶于水
⑤H2在Cl2中燃烧
⑥弱酸电离
⑦NH4Cl晶体与Ba(OH)2?8H2O混合搅拌.
①液态水变成水蒸气
②酸碱中和反应
③浓H2SO4稀释
④固体氢氧化钠溶于水
⑤H2在Cl2中燃烧
⑥弱酸电离
⑦NH4Cl晶体与Ba(OH)2?8H2O混合搅拌.
| A、②③④ | B、①⑥⑦ |
| C、①③⑤ | D、②③④⑤ |
下列事实不能用勒夏特列原理解释的是( )
| A、黄绿色的氯水光照后颜色变浅 |
| B、NO2(g)+SO2(g)?SO3(g)+NO(g),对该平衡体系加压后颜色加深 |
| C、由NO2和N2O4组成的平衡体系加压后颜色先变深后变浅 |
| D、在含有Fe(SCN)3的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去 |
在25℃和1.01×105Pa时,2N2O5(g)=4NO2(g)+O2(g);△H=+56.7kJ/mol,能自发进行的合理解释是( )
| A、是吸热反应 |
| B、是放热反应 |
| C、是熵减反应 |
| D、是熵增效应大于能量效应 |
下列方程式中,属于水解反应的是( )
| A、H2O+H2O?H3O++OH- |
| B、HCO3-+H2O?H2CO3+OH- |
| C、HCO3-+H2O?H3O++CO32- |
| D、HCO3-+OH-?H2O+CO32- |



