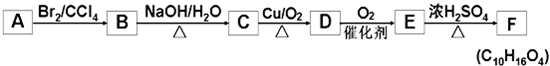
题目内容
下列方程式中,属于水解反应的是( )
| A、H2O+H2O?H3O++OH- |
| B、HCO3-+H2O?H2CO3+OH- |
| C、HCO3-+H2O?H3O++CO32- |
| D、HCO3-+OH-?H2O+CO32- |
考点:盐类水解的原理
专题:盐类的水解专题
分析:弱离子水解反应的实质是:弱离子和水电离出的氢离子或氢氧根离子结合生成弱电解质的过程,水解方程式用可逆号.
解答:
解:A、H2O+H2O?H3O++OH-是水的电离方程式,故A错误;
B、碳酸氢根水解会生成碳酸和氢氧根,故B正确;
C、HCO3-+H2O?H3O++CO32-是碳氢根离子的电离方程式,故C错误;
D、该过程是碳酸氢根离子和氢氧根离子之间反应的过程,属于发生的化学反应,不属于水解反应,故D错误;
故选:B.
B、碳酸氢根水解会生成碳酸和氢氧根,故B正确;
C、HCO3-+H2O?H3O++CO32-是碳氢根离子的电离方程式,故C错误;
D、该过程是碳酸氢根离子和氢氧根离子之间反应的过程,属于发生的化学反应,不属于水解反应,故D错误;
故选:B.
点评:本题考查盐类水解原理,水解离子方程式的分析判断,注意电离方程式的理解应用,特别是写成水合氢离子的电离方程式的判断,题目难度中等.

练习册系列答案
相关题目
下表是五种银盐的溶度积常数Ksp(25℃),下列说法不正确的是( )
| 化学式 | AgCl | Ag2SO4 | Ag2S | AgBr | AgI |
| 溶度积 | 1.4×10-10 | 1.4×10-5 | 6.3×10-50 | 7.7×10-13 | 8.51×10-16 |
| A、25℃时五种银盐的饱和溶液中,c(Ag+)最大的是Ag2SO4溶液 |
| B、在氯化银的悬浊液中加入Na2S溶液可以生成黑色的Ag2S |
| C、25℃时,在等物质的量浓度的NaCl、CaCl2两溶液中加入足量的AgCl固体形成饱和溶液,则两溶液中AgCl的溶度积相同,且两溶液中c(Ag+)也相同 |
| D、AgBr沉淀可以转化成AgI沉淀,而 AgI沉淀在一定条件下也可以转化成AgBr沉淀 |
下列关于化学与环境的叙述不正确的是( )
| A、航天飞机上的隔离陶瓷属于复合材料 |
| B、CO2和NO2是造成酸雨的主要原因 |
| C、燃煤中加入适量石灰石,可减少废气中SO2的含量 |
| D、垃圾是放错地方的资源,应分类回收利用 |
已知化学反应A2(g)+B2(g)═2AB(g)△H=Q kJ?mol-1,其能量变化如图所示,则Q的值正确的是( )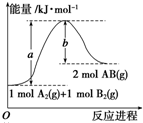

| A、a-b | B、a | C、-b | D、b-a |
 二茂铁[(C5H5)2Fe]分子是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等.它的结构如下图所示,下列说法正确的是( )
二茂铁[(C5H5)2Fe]分子是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等.它的结构如下图所示,下列说法正确的是( )| A、二茂铁中Fe2+与环戊二烯离子(C5H5-)之间为离子键 |
B、1mol环戊二烯(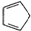 )中含有σ键的数目为5NA )中含有σ键的数目为5NA |
| C、分子中存在π键 |
| D、Fe2+的电子排布式为1s22s22p63s23p63d44s2 |
某元素在化学反应中由化合态变为游离态,则该元素( )
| A、一定被氧化 |
| B、一定被还原 |
| C、可能被氧化也可能被还原 |
| D、既没被氧化也没被还原 |