题目内容
根据下列化学方程式,判断有关物质的还原性强弱的顺序为( )
①I2+SO2+2H2O═H2SO4+2HI;
②2FeCl2+Cl2═2FeCl3;
③2FeCl3+2HI═2FeCl2+2HCl+I2.
①I2+SO2+2H2O═H2SO4+2HI;
②2FeCl2+Cl2═2FeCl3;
③2FeCl3+2HI═2FeCl2+2HCl+I2.
| A、I->Fe2+>Cl->SO2 |
| B、Cl->Fe2+>SO2>I- |
| C、Fe2+>I->Cl->SO2 |
| D、SO2>I->Fe2+>Cl- |
考点:氧化性、还原性强弱的比较
专题:
分析:同一自发进行的氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性,还原剂的还原性大于还原产物的还原性,据此分析解答.
解答:
解:①I2+SO2+2H2O═2HI+H2SO4中还原剂是SO2、还原产物是HI,所以还原性SO2>HI;
②2FeCl2+Cl2═2FeCl3中还原剂是FeCl2、还原产物是FeCl3,所以还原性FeCl2>FeCl3;
③2FeCl3+2HI═2FeCl2+2HCl+I2中还原剂是HI、还原产物是FeCl2,所以还原性HI>FeCl2;
通过以上分析知,还原性强弱顺序是SO2>I->Fe2+>Cl-,
故选D.
②2FeCl2+Cl2═2FeCl3中还原剂是FeCl2、还原产物是FeCl3,所以还原性FeCl2>FeCl3;
③2FeCl3+2HI═2FeCl2+2HCl+I2中还原剂是HI、还原产物是FeCl2,所以还原性HI>FeCl2;
通过以上分析知,还原性强弱顺序是SO2>I->Fe2+>Cl-,
故选D.
点评:本题考查还原性强弱判断,侧重考查学生对基本概念的理解,根据元素化合价变化分析解答即可,知道常见元素化合价,题目难度不大.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
下列物质,既能和稀H2SO4溶液反应又能和NaOH溶液反应的是( )
①
②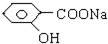
③AL(OH)3
④NaHCO3
⑤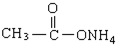
①

②

③AL(OH)3
④NaHCO3
⑤
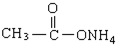
| A、全部 | B、仅①②③④ |
| C、仅①④⑤ | D、仅①②③ |
已知化学反应A2(g)+B2(g)═2AB(g)△H=Q kJ?mol-1,其能量变化如图所示,则Q的值正确的是( )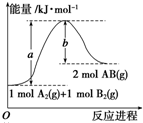

| A、a-b | B、a | C、-b | D、b-a |
在25℃和1.01×105Pa时,2N2O5(g)=4NO2(g)+O2(g);△H=+56.7kJ/mol,能自发进行的合理解释是( )
| A、是吸热反应 |
| B、是放热反应 |
| C、是熵减反应 |
| D、是熵增效应大于能量效应 |
某元素在化学反应中由化合态变为游离态,则该元素( )
| A、一定被氧化 |
| B、一定被还原 |
| C、可能被氧化也可能被还原 |
| D、既没被氧化也没被还原 |
下列事实与胶体性质无关的是( )
| A、可用半透膜除去淀粉溶液中的少量NaCl |
| B、黄河入海口容易形成沙洲 |
| C、将植物油倒入水中用力搅拌可形成油水混合物 |
| D、一束平行光线通过蛋白质溶液,从侧面可以看到一条光亮的通路 |
决定一定物质的量的气体体积大小的主要因素有( )
| A、气体分子的直径 |
| B、气体分子的数目 |
| C、气体分子间距离 |
| D、气体分子的相对分子质量 |
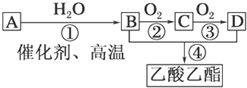 根据所给信息填空
根据所给信息填空