题目内容
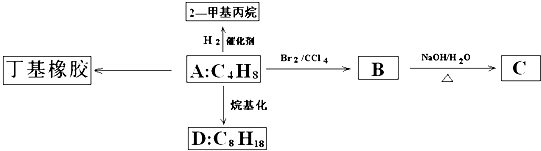
反应 A+B→C(△H<0)分两步进行:①A+B→X (△H>0),②X→C(△H<0).下列示意图中,能正确表示总反应过程中能量变化的是( )
A、 |
B、 |
C、 |
D、 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:根据物质具有的能量进行计算:△H=E(生成物的总能量)-E(反应物的总能量),当反应物的总能量大于生成物的总能量时,反应放热,当反应物的总能量小于生成物的总能量时,反应吸热,以此解答该题.
解答:
解:由反应 A+B→C(△H<0)分两步进行 ①A+B→X (△H>0)②X→C(△H<0)可以看出,A+B→C(△H<0)是放热反应,A和B的能量之和大于C,由①A+B→X (△H>0)可知这步反应是吸热反应,X→C(△H<0)是放热反应,故X的能量大于A+B;A+B的能量大于C;X 的能量大于C,图象B符合,
故选D.
故选D.
点评:本题为图象题,主要考查了物质的能量分析应用,化学反应的能量变化、分析,题目难度不大,注意反应热与物质总能量大小的关系判断.

练习册系列答案
相关题目
误食重金属盐会引起中毒,下列不能用于解毒的措施是( )
| A、服大量鸡蛋清 |
| B、喝大量豆浆 |
| C、喝大量牛奶 |
| D、喝食盐水 |
下列说法正确的是( )


| A、图(a)中,随着电解的进行,溶液中H+的浓度越来越小 |
| B、图(b)中,Mg电极作电池的负极 |
| C、图(c)中,发生的反应为Co+Cd2+=Cd+Co2+ |
| D、图(d)中,K分别与M、N连接时,Fe电极均受到保护 |
下列有关热化学方程式的叙述正确的是( )
| A、已知2H2(gO2(g)=2H2O(g);△H=-483.6 kJ/mol,则氢气的燃烧热为241.8 kJ/mol |
| B、已知C(石墨,s)=C(金刚石,s);△H>0,则金刚石比石墨稳定 |
| C、含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则该反应中和热的热化学方程式为:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(aq);△H=-57.4 kJ/mol |
| D、已知2C(s)+2O2(g)=2CO2(g);△H1,2C(s)+O2(g)=2CO(g);△H2.则△H1<△H2 |
同主族元素所形成的同一类化合物,往往其结构和性质相似.化合物PH4I是一种无色晶体,下列对它的描述错误的是( )
| A、是一种共价化合物 |
| B、可由PH3与HI化合生成 |
| C、在加热的条件下,可以分解产生有色气体 |
| D、能跟碱反应放出PH3 |
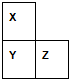 X、Y、Z、W、R是短周期元素,X、Y、Z在周期表中的位置如图所示,其中Z的族序数与周期序数之差为4,W最高价氧化物水化物的阴、阳离子电子数相等,R与W同周期,R最高价氧化物的水化物与W、Y最高价氧化物的水化物均能反应.
X、Y、Z、W、R是短周期元素,X、Y、Z在周期表中的位置如图所示,其中Z的族序数与周期序数之差为4,W最高价氧化物水化物的阴、阳离子电子数相等,R与W同周期,R最高价氧化物的水化物与W、Y最高价氧化物的水化物均能反应.