下列对沉淀溶解平衡的描述正确的是( )
| A、反应开始时,溶液中各离子浓度相等 |
| B、达到平衡时,沉淀的速率和溶解的速率相等 |
| C、达到平衡时,溶液中溶质的离子浓度相等,且保持不变 |
| D、达到平衡时,如果再加入难溶性的该沉淀物,将促进溶解 |
常温常压下,现有浓度为0.100mol/L的六种溶液:①HCl,②H2SO4,③CH3COOH,④CH3COONa ⑤NaOH,⑥Na2CO3由水电离出的C(H+)大小关系正确的是( )
| A、⑥>④>③>①=⑤>② |
| B、①=②>③>⑥>④>⑤ |
| C、②>①>③>④>⑥>⑤ |
| D、④>⑥>③>①=⑤>② |
下列性质中,不能说明乙酸是弱电解质的是( )
| A、乙酸钠溶液显碱性 |
| B、常温时,0.1 mol?L-1乙酸溶液的pH约为3 |
| C、10mL 1mol?L-1乙酸溶液与10mL1mol?L-1的NaOH溶液恰好完全反应 |
| D、在相同温度下,同物质的量浓度的乙酸溶液的导电性比甲酸(为弱酸)溶液的弱 |
在一定温度下,氯化银在水中存在如下沉淀溶解平衡:AgCl(s)?Ag+(aq)+Cl-(aq),若把AgCl分别放入①100mL0.1mol/LNa2SO4溶液中;②100mL0.1mol/L NaCl溶液中;③100mL0.1mol/L AlCl3溶液中;④100mL0.1mol/L MgCl2溶液中.搅拌后在相同的温度下Ag+浓度由大到小的顺序是( )
| A、①>②>④>③ |
| B、②>①>④>③ |
| C、④>③>②>① |
| D、①>④>③>② |
常温下,现有1mL c1 mol/L的醋酸溶液和1mL c2mol/L的氢氧化钠溶液.下列说法中正确的是( )
| A、若c1=c2,则醋酸溶液中的c(H+)与氢氧化钠溶液中的c(OH-)相同 |
| B、若醋酸溶液的pH=3,氢氧化钠溶液的pH=11,则醋酸溶液中的c(CH3COO-)与氢氧化钠钠溶液中的c(Na+)相同 |
| C、将醋酸溶液与氢氧化钠溶液混合,若c1=c2,则所得溶液的pH=7 |
| D、将醋酸溶液与氢氧化钠溶液混合,若所得混合溶液的pH=7,则混合液中c(CH3COO-)>c(Na+) |
将0.3mol硝酸银、0.6mol硝酸铜、0.7mol氯化钾溶于水,配成100mL溶液,用惰性电极电解一段时间后,若在一极析出0.4mol铜,此时在另一极上产生的气体体积(标准状况)为多少( )
| A、4.48L | B、5.6L |
| C、6.72L | D、8.96L |
下列离子在溶液中能大量共存的是( )
| A、HCO3-、Ba2-、SO42-、H+ |
| B、K+、SiO32-、H+、Cl- |
| C、Fe3+、OH-、NO3-、HCO3- |
| D、Al3+、H+、NO3-、SO42- |
溴(Br)与氯同属“卤族”元素,其单质在性质上具有很大的相似性,但Cl2比Br2的活泼性强,下面是根据的氯性质对溴的性质的预测,其中不正确的是( )
| A、溴单质常温下为液态,但极容易挥发为溴蒸气 |
| B、溴单质只具有氧化性 |
| C、溴原子外层有7个电子,在化学反应中容易得1个电子,表现氧化性 |
| D、溴离子可以用酸性AgNO3溶液来检验 |

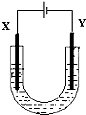 如图是用石墨和铁作电极电解饱和食盐水的装置,请填空:
如图是用石墨和铁作电极电解饱和食盐水的装置,请填空: