题目内容
溴(Br)与氯同属“卤族”元素,其单质在性质上具有很大的相似性,但Cl2比Br2的活泼性强,下面是根据的氯性质对溴的性质的预测,其中不正确的是( )
| A、溴单质常温下为液态,但极容易挥发为溴蒸气 |
| B、溴单质只具有氧化性 |
| C、溴原子外层有7个电子,在化学反应中容易得1个电子,表现氧化性 |
| D、溴离子可以用酸性AgNO3溶液来检验 |
考点:氯、溴、碘及其化合物的综合应用
专题:
分析:Cl2比Br2的活泼性强,但二者性质相似,均与水、碱发生氧化还原反应,对应离子均与硝酸银溶液反应生成沉淀,以此来解答.
解答:
解:A.溴沸点较高,常温下为液态,易挥发,故A正确;
B.溴单质中溴元素化合价为0价,处于中间价态,具有氧化性也具有还原性,故B错误;
C.溴原子最外层有7个电子,在化学反应中容易得到一个电子形成稳定的溴离子,故C正确;
D.溴离子可以用硝酸酸化的AgNO3溶液来检验,生成不溶于硝酸的AgBr浅黄色沉淀,故D正确;
故选B.
B.溴单质中溴元素化合价为0价,处于中间价态,具有氧化性也具有还原性,故B错误;
C.溴原子最外层有7个电子,在化学反应中容易得到一个电子形成稳定的溴离子,故C正确;
D.溴离子可以用硝酸酸化的AgNO3溶液来检验,生成不溶于硝酸的AgBr浅黄色沉淀,故D正确;
故选B.
点评:本题考查卤素单质的性质,为高频考点,把握性质的相似性为解答的关键,注意把握类推法分析解答,侧重元素化合物知识的考查,题目难度不大.

练习册系列答案
相关题目
下列家庭化学小实验能达到预期目的是( )
| A、用米汤检验食用加碘盐(含KIO3)中含有碘 |
| B、用碘酒检验汽油中是否含有不饱和烃 |
| C、提纯蛋白质可以在蛋白质溶液中加饱和CuSO4溶液,蛋白质析出,然后把沉淀溶于蒸馏水中 |
| D、淀粉溶液中加入硫酸加热水解,冷却,加银氨溶液做银镜反应 |
人类应以可持续发展的方式使用资源,以合理的方式对废物进行处理并循环使用,下列做法不利于环境保护的是( )
| A、回收并合理处理废电池 |
| B、将煤转化为水煤气作燃料 |
| C、发电厂的煤经脱硫处理 |
| D、电镀废液经中和后直接排放 |
下列性质中,不能说明乙酸是弱电解质的是( )
| A、乙酸钠溶液显碱性 |
| B、常温时,0.1 mol?L-1乙酸溶液的pH约为3 |
| C、10mL 1mol?L-1乙酸溶液与10mL1mol?L-1的NaOH溶液恰好完全反应 |
| D、在相同温度下,同物质的量浓度的乙酸溶液的导电性比甲酸(为弱酸)溶液的弱 |
水的电离过程为H2O?H++OH-,在不同温度下其离子积为:Kw(25℃)=1×10-14,Kw(35℃)=2.1×10-14.则下列叙述正确的是( )
| A、c(H+)随着温度的升高而降低 |
| B、在35℃时,纯水中 c(H+)>c(OH-) |
| C、水的电离常数K(25℃)>K(35℃) |
| D、水的电离是一个吸热过程 |
每年的6月26日是国际禁毒日.以下是四种毒品的结构简式,下列有关说法正确的是( )
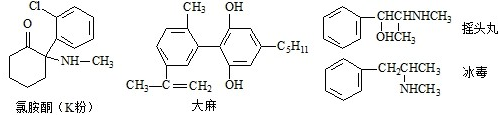

| A、四种毒品中都含有苯环,都属于芳香烃 |
| B、摇头丸经消去、加成反应可制得冰毒 |
| C、1mol大麻与溴水反应最多消耗4mol Br2 |
| D、氯胺酮分子中环上所有碳原子可能共平面 |
下列各组中都是酸性食物的是( )
| A、猪肉 大米 苹果 花生 |
| B、豆腐 鸡肉 面包 小麦 |
| C、玉米 海带 西瓜 面粉 |
| D、大麦 玉米 牛肉 蛋黄 |