题目内容
下列性质中,不能说明乙酸是弱电解质的是( )
| A、乙酸钠溶液显碱性 |
| B、常温时,0.1 mol?L-1乙酸溶液的pH约为3 |
| C、10mL 1mol?L-1乙酸溶液与10mL1mol?L-1的NaOH溶液恰好完全反应 |
| D、在相同温度下,同物质的量浓度的乙酸溶液的导电性比甲酸(为弱酸)溶液的弱 |
考点:弱电解质的判断
专题:
分析:弱电解质在水溶液里部分电离,只要说明乙酸在水溶液里部分电离就能证明乙酸是弱电解质,可以根据一定浓度的pH、其钠盐溶液酸碱性等判断.
解答:
解:A.乙酸钠溶液显碱性,说明乙酸钠是强碱弱酸盐,则证明乙酸是弱酸,为弱电解质,故A不选;
B.常温时,0.1 mol?L-1乙酸溶液的pH约为3,溶液中氢离子浓度小于酸浓度,说明乙酸不完全电离为弱电解质,故B不选;
C.10mL 1mol?L-1乙酸溶液与10mL1mol?L-1的NaOH溶液恰好完全反应,说明乙酸是一元酸不能说明乙酸部分电离,所以不能证明乙酸是弱电解质,故C选;
D.相同温度下,同物质的量浓度的乙酸溶液的导电性比甲酸(为弱酸)溶液的弱,说明乙酸电离程度小于甲酸,甲酸是弱酸,则乙酸也是弱酸,故D不选;
故选C.
B.常温时,0.1 mol?L-1乙酸溶液的pH约为3,溶液中氢离子浓度小于酸浓度,说明乙酸不完全电离为弱电解质,故B不选;
C.10mL 1mol?L-1乙酸溶液与10mL1mol?L-1的NaOH溶液恰好完全反应,说明乙酸是一元酸不能说明乙酸部分电离,所以不能证明乙酸是弱电解质,故C选;
D.相同温度下,同物质的量浓度的乙酸溶液的导电性比甲酸(为弱酸)溶液的弱,说明乙酸电离程度小于甲酸,甲酸是弱酸,则乙酸也是弱酸,故D不选;
故选C.
点评:本题考查弱电解质的判断,明确强弱电解质的根本区别是解本题关键,电解质强弱只与电离程度有关,与电解质溶解性无关,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
白色污染的危害主要有( )
①破坏土壤结构、降低土壤肥效 ②焚烧产生有毒气体,污染环境 ③释放出氟氯代烷破坏臭氧层 ④危害动物 ⑤加剧温室效应 ⑥引起赤潮.
①破坏土壤结构、降低土壤肥效 ②焚烧产生有毒气体,污染环境 ③释放出氟氯代烷破坏臭氧层 ④危害动物 ⑤加剧温室效应 ⑥引起赤潮.
| A、全部 | B、①②③④⑤ |
| C、③④⑤⑥ | D、①②⑤⑥ |
溴(Br)与氯同属“卤族”元素,其单质在性质上具有很大的相似性,但Cl2比Br2的活泼性强,下面是根据的氯性质对溴的性质的预测,其中不正确的是( )
| A、溴单质常温下为液态,但极容易挥发为溴蒸气 |
| B、溴单质只具有氧化性 |
| C、溴原子外层有7个电子,在化学反应中容易得1个电子,表现氧化性 |
| D、溴离子可以用酸性AgNO3溶液来检验 |
下列说法正确的是( )
| A、将氯化铝溶液加热,蒸干后得到无水氯化铝固体 |
| B、向Fe(OH)3胶体通电,发现胶体向正极移动,根据电场的作用,我们可以得出,Fe(OH)3带负电 |
| C、23Na37Cl中的质子数和中子数之比7:8 |
| D、硝酸铝溶液中滴加少量的氢氧化钠生成Al(OH)3 |
氯水不稳定,要现用现配,下列吸收氯气制备氯水的装置最合理的是( )
A、 |
B、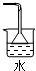 |
C、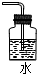 |
D、 |