常温下,下列溶液中酸性最弱的是( )
| A、pH=4 |
| B、[H+]=1×10-3 mol?L-1 |
| C、[OH-]=1×10-11 mol?L-1 |
| D、[H+]?[OH-]=1×10-14 |
下列化学反应既属于离子反应又是氧化还原反应的是( )
| A、大理石与稀盐酸 |
| B、硝酸银溶液与氯化钠溶液 |
| C、锌粒与稀硫酸 |
| D、红热木炭跟水蒸气反应 |
常温下,0.1mol?L-1某一元酸(HA)溶液中
=1×10-8,下列叙述正确的是( )
| c(OH-) |
| c(H+) |
| A、溶液中水电离出的c(H+)=10-10mol?L-1 |
| B、溶液中c(H+)+c(A-)=0.1 mol?L-1 |
| C、与0.05 mol?L-1NaOH溶液等体积混合后所得溶液中离子浓度大小关系为:c(A-)>c(Na+)>c(OH-)>c(H+) |
| D、上述溶液中加入一定量CH3COONa晶体或加水稀释,溶液c(OH-)均增大 |
酒后驾车人员体内酒精含量的检测装置如图所示,下列说法不正确的是( )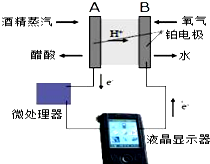

| A、电极B是正极,该电极反应为O2+2H2O+4e-═4OH- |
| B、电极A的反应:H2O+C2H5OH-4e-═CH3COOH+4H+ |
| C、该检测装置实现了将化学能转化为电能,且单位时间内通过电量越大,酒精含量越高 |
| D、电池反应:O2+C2H5OH═CH3COOH+H2O |
下列离子中,核外有10个电子的是( )
| A、Mg2+ |
| B、S2- |
| C、K+ |
| D、Cl- |
工业上由二氧化锰制备高锰酸钾可分二步进行,第一步:二氧化锰与氢氧化钾共熔并通入氧气2MnO2+4KOH+O2
2K2MnO4+2H2O;第二步:电解锰酸钾溶液:2K2MnO4+2H2O
2KMnO4+H2↑+2KOH则下列说法正确的是( )
| ||
| ||
| A、根据上述过程,每生成1molKMnO4,共转移6mol电子 | ||||
B、第二步电解时,阳极电极反应式为2MnO
| ||||
C、第二步电解的离子方程式为:2H2O
| ||||
| D、第二步电解时阴极周围pH减小 |