题目内容
酒后驾车人员体内酒精含量的检测装置如图所示,下列说法不正确的是( )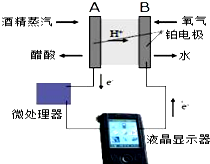

| A、电极B是正极,该电极反应为O2+2H2O+4e-═4OH- |
| B、电极A的反应:H2O+C2H5OH-4e-═CH3COOH+4H+ |
| C、该检测装置实现了将化学能转化为电能,且单位时间内通过电量越大,酒精含量越高 |
| D、电池反应:O2+C2H5OH═CH3COOH+H2O |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:该装置是燃料电池,属于原电池,投放燃料的电极是负极,投放氧化剂的电极是正极,负极上乙醇失电子生成乙酸,正极上氧气得电子发生还原反应,所以该电池反应是乙醇被氧化生成乙酸和水.
解答:
解:A、原电池投放氧化剂的电极是正极,正极上氧气得电子和氢离子反应生成水,溶液中氢离子浓度减小,pH增大,故A错误;
B、该原电池中,投放酒精的电极是负极,负极上乙醇失电子和水反应生成乙酸和氢离子,电极反应式为:H2O+C2H5OH-4e-=CH3COOH+4H+,故B正确;
C、该装置是将化学能转变为电能的装置,属于原电池,原电池放电时,单位时间内通过电量越大,需要的燃料越多,则酒精含量越高,故C正确;
D、该原电池的反应是乙醇被氧化生成乙酸和水,电池反应式为O2+C2H5OH=CH3COOH+H2O,故D正确.
故选A.
B、该原电池中,投放酒精的电极是负极,负极上乙醇失电子和水反应生成乙酸和氢离子,电极反应式为:H2O+C2H5OH-4e-=CH3COOH+4H+,故B正确;
C、该装置是将化学能转变为电能的装置,属于原电池,原电池放电时,单位时间内通过电量越大,需要的燃料越多,则酒精含量越高,故C正确;
D、该原电池的反应是乙醇被氧化生成乙酸和水,电池反应式为O2+C2H5OH=CH3COOH+H2O,故D正确.
故选A.
点评:本题考查了原电池原理,书写燃料电池的电极反应式要结合电解质溶液的酸碱性,燃料和氧化剂相同,电解质溶液不同,则电极反应式也不同.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
如图所示对实验仪器名称的标注或实验操作正确的是( )
A、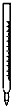 酸式滴定管 |
B、 氨气的制取 |
C、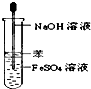 Fe(OH)2的制取 |
D、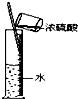 浓硫酸稀释 |
对于淀粉和纤维素两种物质,下列说法正确的是( )
| A、二者都能水解,且水解的最终产物相同 |
| B、二者含有C、H、O三种元素的质量分数相同,因为互为同分异构体 |
| C、他们均属于糖类,且都是高分子化合物 |
| D、都可用(C6H10O5)n表示,但淀粉能发生银镜反应而纤维素不能 |
下列说法正确的是( )
| A、相对分子质量相同的物质是同种物质 |
| B、相对分子质量相差14的两种有机物,一定是属于同系物 |
| C、分子式相同的不同有机物一定是同分异构体 |
| D、分子中含有碳与氢元素的化合物是烃类 |
下列有关金属冶炼的说法中错误的是( )
| A、炼铁中加入焦炭作造渣剂 |
| B、炼钢中吹入氧气作氧化剂 |
| C、电解铝生产中加入冰晶石以降低氧化铝的熔点 |
| D、火法冶金比湿法冶金能耗大 |
下列化学反应既属于离子反应又是氧化还原反应的是( )
| A、大理石与稀盐酸 |
| B、硝酸银溶液与氯化钠溶液 |
| C、锌粒与稀硫酸 |
| D、红热木炭跟水蒸气反应 |
下列物质的水溶液pH最大的是( )
| A、NaHCO3 |
| B、KHSO4 |
| C、AlCl3 |
| D、CH3COONa |
关于钠及其化合物性质的叙述,不正确的是( )
| A、过氧化钠是淡黄色固体,可用于呼吸面具中作为氧气的来源 |
| B、氧化钠和过氧化钠都能与二氧化碳反应,生成物完全相同 |
| C、碳酸钠固体中混有少量碳酸氢钠,可用加热的方法除去 |
| D、质量相等的碳酸钠和碳酸氢钠分别与足量盐酸反应,后者产生气体多 |
下列说法中正确的是( )
| A、固体的溶解过程只与焓变有关 |
| B、反应焓变是决定反应能否自发进行的唯一因素 |
| C、温度、压强一定时,焓因素和熵因素共同决定一个化学反应的方向 |
| D、某一化学反应的△H>0和△S>0,则该反应一定自发进行 |