��Ŀ����
��ҵ���ɶ��������Ʊ�������ؿɷֶ������У���һ���������������������ع��۲�ͨ������2MnO2+4KOH+O2
2K2MnO4+2H2O���ڶ���������������Һ��2K2MnO4+2H2O
2KMnO4+H2��+2KOH������˵����ȷ���ǣ�������
| ||
| ||
| A�������������̣�ÿ����1molKMnO4����ת��6mol���� | ||||
B���ڶ������ʱ�������缫��ӦʽΪ2MnO
| ||||
C���ڶ����������ӷ���ʽΪ��2H2O
| ||||
| D���ڶ������ʱ������ΧpH��С |
���㣺���ԭ��,������ԭ��Ӧ
ר�⣺
������A�����ݸ�����غ�ת�Ƶ���֮��Ĺ�ϵʽ���㣻
B�����ʱ��������ʧ���ӷ���������Ӧ��
C���ڶ����������ӷ���ʽΪ��2MnO42-+H2O
2MnO4-+H2��+2OH-��
D�����ʱ�������ϵõ��ӷ�����ԭ��Ӧ��
B�����ʱ��������ʧ���ӷ���������Ӧ��
C���ڶ����������ӷ���ʽΪ��2MnO42-+H2O
| ||
D�����ʱ�������ϵõ��ӷ�����ԭ��Ӧ��
���
�⣺A��������ʽ2MnO2+4KOH+O2
2K2MnO4+2H2O��2K2MnO4+H2O
2KMnO4+H2��+2KOH��ӵ�2MnO2+4KOH+O2=2KMnO4+H2��+2KOH+H2O��ÿ����1mol KMnO4��ת�Ƶ��ӵ����ʵ���=1mol��7-4��=3mol����A����
B���ڶ������ʱ���������������ʧ�������ɸ�����أ������缫��ӦʽΪ2MnO42--2e-=2MnO4-����B��ȷ��
C���ڶ����������ӷ���ʽΪ��2MnO42-+H2O
2MnO4-+H2��+2OH-����C����
D���ڶ������ʱ�������������ӵõ����������������������������������������ɣ�����ҺpH����D����
��ѡB��
| ||
| ||
B���ڶ������ʱ���������������ʧ�������ɸ�����أ������缫��ӦʽΪ2MnO42--2e-=2MnO4-����B��ȷ��
C���ڶ����������ӷ���ʽΪ��2MnO42-+H2O
| ||
D���ڶ������ʱ�������������ӵõ����������������������������������������ɣ�����ҺpH����D����
��ѡB��
���������⿼����������ԭ��Ӧ�����ԭ������ȷ���ʱ�����Ϸŵ�����Ӽ�Ԫ�ػ��ϼ��ǽⱾ��ؼ����Ѷ��еȣ�

��ϰ��ϵ�д�
 ��˼ά������ҵ��ټ��ִ�ѧ������ϵ�д�
��˼ά������ҵ��ټ��ִ�ѧ������ϵ�д� �����������Ż�ѧϰϵ�д�
�����������Ż�ѧϰϵ�д�
�����Ŀ
�����������ij���Ԫ�أ�������ÿ����Ҫ800mg�ĸƣ����в��Ƶķ�ʽ����ȷ���ǣ�������
| A������ɹ̫�� |
| B���������ø����Ӻ����ߵ�Ӳˮ |
| C����������ţ�̡����� |
| D����������D |
 ����������ͼ��ʾ�����㷺Ӧ���ڷ��������������Ʒ�У���ɱ�����������ã������й���������˵������ȷ���ǣ�������
����������ͼ��ʾ�����㷺Ӧ���ڷ��������������Ʒ�У���ɱ�����������ã������й���������˵������ȷ���ǣ�������| A���������������Ը��������Һ����������Ӧ |
| B����������������ˮ����ȡ����Ӧ |
| C���������ķ���ʽΪC12H7O2Cl3 |
| D����������һ��±���� |
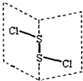 ���Ȼ���S2Cl2���㷺������ҵ�����ӽṹ��ͼ�������£�S2Cl2��һ�ֳȻ�ɫҺ�壬��ˮѸ�ٷ�Ӧ����������ʹƷ����ɫ�����壮����˵����ȷ���ǣ�������
���Ȼ���S2Cl2���㷺������ҵ�����ӽṹ��ͼ�������£�S2Cl2��һ�ֳȻ�ɫҺ�壬��ˮѸ�ٷ�Ӧ����������ʹƷ����ɫ�����壮����˵����ȷ���ǣ�������A��S2Cl2�ĵ���ʽ��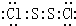 |
| B��S2Cl2Ϊ���м��Լ��ͷǼ��Լ��ķǼ��Է��� |
| C��S2Br2��S2Cl2�ṹ���ƣ��۷е㣺S2Br2��S2Cl2 |
| D��S2Cl2��H2O��Ӧ��ѧ����ʽ����Ϊ��2 S2Cl2+2H2O=SO2��+3S��+4HCl |
�������Ӽ��ܵ�������ˮ�⣬������ǿ����Һ��Ӧ���ǣ�������
| A��CH3COO- |
| B��HSO4- |
| C��HSO3- |
| D��CO32- |
���и�������ʾ��ͼһ�µ��ǣ�������
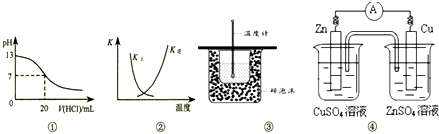

| A��ͼ�ٱ�ʾ25��ʱ����0.1 mol?L-1����ζ�20 mL 0.1 mol?L-1 NaOH��Һ����Һ��pH�����������ı仯 |
| B��ͼ�������߱�ʾ��Ӧ2SO2��g��+O2��g��?2SO3��g������H��0 �����淴Ӧ��ƽ�ⳣ��K���¶ȵı仯 |
| C��ͼ��װ�����ڲⶨ�к��� |
| D��ͼ��װ�ÿ��Թ���п��ͭ������ͭ��Һԭ��� |