一个原电池的总反应为Zn+Cu2+=Zn2++Cu,该反应的原电池的正确组成是( )
| A、正极 Zn 负极 Cu 电解质溶液 CuCl2 |
| B、正极Cu 负极Zn 电解质溶液 CuCl2 |
| C、正极Zn 负极Cu 电解质溶液 ZnCl2 |
| D、正极Cu 负极Zn 电解质溶液 ZnCl2 |
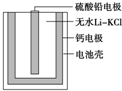 如图为一种热激活电池的基本结构,该电池总反应为PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.作为电解质的无水LiClKCl混合物受热熔融后,电池即可瞬间输出电能.下列有关说法正确的是( )
如图为一种热激活电池的基本结构,该电池总反应为PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.作为电解质的无水LiClKCl混合物受热熔融后,电池即可瞬间输出电能.下列有关说法正确的是( )| A、正极反应式:Ca+2Cl-+2e-═CaCl2 |
| B、放电过程中,Li+向负极移动 |
| C、每转移0.1mol电子,理论上生成20.7gPb |
| D、常温时,在正负极间接上电流表或检流计,指针不偏转 |
合成氨工业对国民经济和社会发展具有重要的意义.其原理为:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol,从化学平衡角度考虑,为了提高氨气的产率,可以选择的方法是( )①升高温度 ②增大压强 ③使用催化剂 ④及时分离出NH3.
| A、①③ | B、①② | C、②③ | D、②④ |
下列关于胶体的叙述中不正确的是( )
| A、丁达尔现象可用来区别胶体与溶液 |
| B、胶体粒子能通过半透膜,不能通过滤纸 |
| C、胶体不稳定,在一定条件下会发生聚沉 |
| D、溶液、胶体、浊液的根本区别是分散质粒子直径的大小 |
氢气在氯气中燃烧产生苍白色火焰,在反应中破坏1mol氢气中的化学键消耗的能量为a KJ,破坏1mol 氯气中的化学键消耗的能量为b KJ,形成1mol氯化氢中的化学键释放的能量为c KJ.下列关系式中正确的是( )
| A、a+b>c |
| B、a+b>2c |
| C、a+b<c |
| D、a+b<2c |
将50ml 1mol/LNaOH溶液加水稀释到500ml,稀释后溶液中NaOH的物质的量浓度是( )
| A、0.1mol/L |
| B、0.5 mol/L |
| C、0.01mol/L |
| D、0.05 mol/L |
某元素的一个原子形成的离子可表示为
Xn-,下列说法正确的是( )
b a |
A、
| ||
B、
| ||
C、X原子的质量数为
| ||
D、X原子的质量约为
|
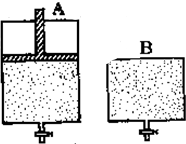 有两只密闭容器A和B.A容器有一个可以移动的活塞能使容器内保持恒压,B容器能保持恒容.起始时向这两个容器中分别充入等物质的量的体积比为2:1的SO2和O2的混合气体,并使A和B容积相等(如图所示).
有两只密闭容器A和B.A容器有一个可以移动的活塞能使容器内保持恒压,B容器能保持恒容.起始时向这两个容器中分别充入等物质的量的体积比为2:1的SO2和O2的混合气体,并使A和B容积相等(如图所示).