欲除去铁粉中混有的少量铝粉,应选用的试剂是( )
| A、稀盐酸 | B、稀硝酸 |
| C、硫酸铜溶液 | D、氢氧化钠溶液 |
称取两份铝粉,第一份加入足量的NaOH溶液,第二份加入足量的盐酸溶液,如果要得到相同体积 (同温同压)的氢气,则两份铝粉的质量比是( )
| A、1:1 | B、1:2 |
| C、3:4 | D、2:5 |
下列反应所产生的气体体积在标准状况下为22.4L的是( )
| A、将2mol金属Cu与含2molH2SO4的浓硫酸共热 |
| B、将1 mol MnO2固体与含4molHCl的浓盐酸共热 |
| C、常温下,将32.2g金属钠和5.4g金属铝同时投入到足量水中 |
| D、常温下,将10.8g的Al和22.4g的Fe投入到300g 98%的硫酸中 |
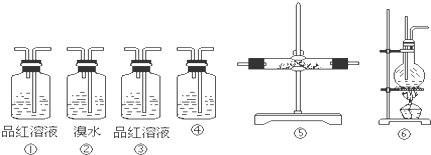
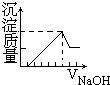
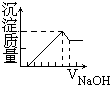
 利用如图装置测定中和热的实验步骤如下:
利用如图装置测定中和热的实验步骤如下: