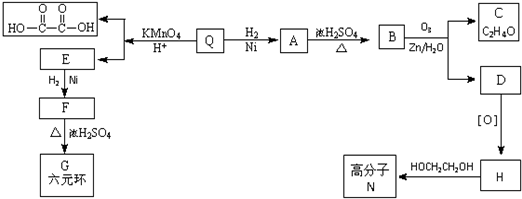
题目内容
欲除去铁粉中混有的少量铝粉,应选用的试剂是( )
| A、稀盐酸 | B、稀硝酸 |
| C、硫酸铜溶液 | D、氢氧化钠溶液 |
考点:铝的化学性质,铁的化学性质
专题:元素及其化合物
分析:铝粉能和强碱反应生成盐和氢气,而铁粉和强碱不反应,据此解题.
解答:
解:铁粉和铝粉都是金属,都具有金属的通性,都能和酸反应和弱碱不反应;但铝粉和铁粉的不同化学性质是:铝粉能和强碱反应生成盐和氢气,而铁粉和强碱不反应,
故选D.
故选D.
点评:本题考查了金属的通性和特性,难度不大,注意:铝是高中化学中唯一能和强酸、强碱反应的金属,可据此性质进行混合物的除杂.

练习册系列答案
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目
100mL 2mol?L-1稀盐酸与一定量的锌充分反应,锌全部溶解,生成的氢气在标准状况下体积为1.12L,设反应后溶液的体积仍为100mL,则反应后溶液中H+物质的量浓度为( )
| A、1.5 mol?L-1 |
| B、1 mol?L-1 |
| C、0.5 mol?L-1 |
| D、0.25 mol?L-1 |
下列离子方程式书写正确的是( )
| A、向CuSO4溶液中加入钠:Na+Cu2+=Cu+Na+ |
| B、向Ba(OH)2溶液中滴加稀盐酸:2H++2Cl-+Ba2++2OH-=2H2O+BaCl2 |
| C、澄清石灰水与盐酸反应:H++OH-=H2O |
| D、往FeCl3溶液中加入Cu粉:2Fe3++3Cu=2Fe+3Cu2+ |
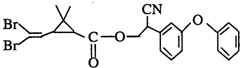 拟除虫菊酯是一类高效、低毒、对昆虫 具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊醋的结构简式如右图:下列对该化合物叙述正确的是( )
拟除虫菊酯是一类高效、低毒、对昆虫 具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊醋的结构简式如右图:下列对该化合物叙述正确的是( )| A、属于芳香烃 |
| B、分子中含有4个手性碳 |
| C、含有3种官能团 |
| D、能发生取代、加成、加聚、氧化、消去反应 |
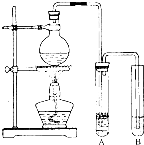 实验室制取少量溴乙烷的装置如图.
实验室制取少量溴乙烷的装置如图.