用于解释下列现象的化学用语表述正确的是( )
| A、硫化钠溶液呈碱性:S2-+2H2O?H2S+2OH- |
| B、亚硫酸溶液呈酸性:H2SO3═2H++SO32- |
| C、FeCl3溶液呈酸性:Fe3++3H2O?Fe(OH)3+3H+ |
| D、氯化铝溶液跟过量的氨水反应:Al3++4OH-═[Al(OH)4]- |
下列离子方程式与所述事实相符且正确的是( )
| A、CuSO4溶液与Ba(OH)2溶液混合:Cu2++SO42-+2OH-+Ba2+═BaSO4↓+Cu(OH)2↓ |
| B、氯化铝溶液中加入过量的氨Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| C、氯化钙与碳酸氢钾溶液混合:Ca2++CO32-═CaCO3↓ |
| D、小苏打与氢氧化钠溶液混合:HCO3-+OH-═CO2↑+H2O |
设nA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、标准状况下,22.4L氯气与过量的铁完全反应,转移电子数为2nA |
| B、42gC3H6中含有的共用电子对数目为8nA |
| C、加热下,1molH2和1molI2混合反应生成的气体分子数为2nA |
| D、0.01mol?L-1的KAl(SO4)2溶液中含有0.02nA个SO42- |
NaCl的摩尔质量是( )
| A、58.5 |
| B、58.5g |
| C、58.5g/mol |
| D、58.5mol |
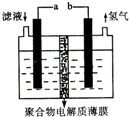 将H2S通人FeCl3溶液中,过滤后将反应液加人电解槽中电解(如图所示)电解后的溶液还可以循环利用.该方法可用于处理石油炼制过程中产生的H2S废气.下列有关说法正确的是( )
将H2S通人FeCl3溶液中,过滤后将反应液加人电解槽中电解(如图所示)电解后的溶液还可以循环利用.该方法可用于处理石油炼制过程中产生的H2S废气.下列有关说法正确的是( )| A、过滤得到的沉淀可能是FeS和S |
| B、若有0.20mol的电子转移,一定能得到2.24L的氢气 |
| C、可以用Fe与外接电源的a极相连 |
| D、与a极相连的电极反应为Fe2+-e-=Fe3+ |
能正确表示下列反应的离子方程式是( )
A、用银氨溶液检验乙醛的醛基:CH3CHO+2Ag(NH3)
| ||||||
B、向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2BrCOOH+OH-
| ||||||
| C、向苯酚钠溶液中通入少量的CO2:CO2+H2O+2C6H5O-→ 2C6H5OH+2CO32- | ||||||
| D、甘氨酸(H2N-CH2-COOH)与氢氧化钠溶液反应:H2N-CH2-COOH+OH-→H2N-CH2COO-+H2O |
以石墨层间化合物氟化石墨为正极,锂为负极,用溶有LiCI04的有机溶剂作电解质新型锂电池,能使输出电压比普通电池提高2倍,该电池具有体积小、重量轻、贮藏性好等特性.电池总反应:nLi+(CF)?nLiF+nC.则下列说法不正确的是( )
| A、放电过程中,Li+从负极区向正极区迁移 |
| B、负极反应式:nLi-ne-?nLi+ |
| C、正极反应式:(CF)n+nLi++ne-?nC+nLiF |
| D、可以用水代替有机溶剂 |
下列关于金属腐蚀的叙述不正确的是( )
| A、黄铜(铜锌合金)制作的铜锣不易产生铜绿 |
| B、与生铁相比纯铁更容易被腐蚀 |
| C、金属的吸氧腐蚀和析氢腐蚀都属于电化学腐蚀 |
| D、金属腐蚀的本质是M-ne?=Mn+ |
NA为阿伏加德罗常数,下列叙述正确的是( )
| A、1L 0.5mol?L-1氨水中所含NH4+数为0.5NA |
| B、1mol Fe与足量氯气反应转移的电子数为2 NA |
| C、标准状况下,33.6L CO2约含有1.5NA个分子 |
D、1 mol  中含碳碳双键数为3 NA 中含碳碳双键数为3 NA |
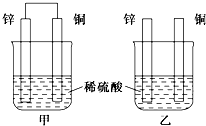 将纯锌片和纯铜片按下图方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
将纯锌片和纯铜片按下图方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题: