题目内容
用于解释下列现象的化学用语表述正确的是( )
| A、硫化钠溶液呈碱性:S2-+2H2O?H2S+2OH- |
| B、亚硫酸溶液呈酸性:H2SO3═2H++SO32- |
| C、FeCl3溶液呈酸性:Fe3++3H2O?Fe(OH)3+3H+ |
| D、氯化铝溶液跟过量的氨水反应:Al3++4OH-═[Al(OH)4]- |
考点:离子方程式的书写
专题:离子反应专题
分析:A.硫离子为多元弱酸根离子,分步水解;
B.亚硫酸为多元弱酸分步电离,用可逆号;
C.三价铁离子为弱碱阳离子水解生成氢氧化铁和氢离子;
D.不符合反应的客观事实,氯化铝与过量氨水反应生成氢氧化铝沉淀和氯化铵.
B.亚硫酸为多元弱酸分步电离,用可逆号;
C.三价铁离子为弱碱阳离子水解生成氢氧化铁和氢离子;
D.不符合反应的客观事实,氯化铝与过量氨水反应生成氢氧化铝沉淀和氯化铵.
解答:
解:A.硫化钠溶液呈碱性,离子方程式:S2-+H2O?HS-+OH-,故A错误;
B.亚硫酸溶液呈酸性,离子方程式:H2SO3 H++HSO3-,故B错误;
C.FeCl3溶液呈酸性,三价铁离子水解的离子方程式:Fe3++3H2O?Fe(OH)3+3H+,故C正确;
D.氯化铝溶液跟过量的氨水反应,离子方程式:Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故D错误;
故选:C.
B.亚硫酸溶液呈酸性,离子方程式:H2SO3 H++HSO3-,故B错误;
C.FeCl3溶液呈酸性,三价铁离子水解的离子方程式:Fe3++3H2O?Fe(OH)3+3H+,故C正确;
D.氯化铝溶液跟过量的氨水反应,离子方程式:Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故D错误;
故选:C.
点评:本题考查了离子方程式的书写,侧重考查盐类的水解和弱电解质的电离,明确电解质的强弱和性质是解题关键,题目难度不大.

练习册系列答案
相关题目
下列物质中,互为同系物的是( )
| A、12C和14C |
| B、乙烷和十六烷 |
| C、葡萄糖和果糖 |
| D、O2和O3 |
下列有关电池的说法不正确的是( )
| A、手机上用的锂离子电池属于二次电池 |
| B、铜锌原电池工作时,电子沿外电路从铜电极流向锌电极 |
| C、铜锌原电池工作时,锌电极发生氧化反应 |
| D、锌锰干电池中,锌电极是负极 |
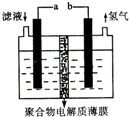 将H2S通人FeCl3溶液中,过滤后将反应液加人电解槽中电解(如图所示)电解后的溶液还可以循环利用.该方法可用于处理石油炼制过程中产生的H2S废气.下列有关说法正确的是( )
将H2S通人FeCl3溶液中,过滤后将反应液加人电解槽中电解(如图所示)电解后的溶液还可以循环利用.该方法可用于处理石油炼制过程中产生的H2S废气.下列有关说法正确的是( )| A、过滤得到的沉淀可能是FeS和S |
| B、若有0.20mol的电子转移,一定能得到2.24L的氢气 |
| C、可以用Fe与外接电源的a极相连 |
| D、与a极相连的电极反应为Fe2+-e-=Fe3+ |
下列离子方程式书写正确的是( )
| A、将一小块钠投入水中Na+H2O=Na++OH-+H2↑ |
| B、硫酸和氢氧化钡混合Ba2++SO42-+H++OH-═BaSO4↓+H2O |
| C、F2和H2O的反应2F2+2H2O=4H++4F-+O2↑ |
| D、将少量NaOH溶液加入Ca(HCO3)2溶液中OH-+HCO3-+Ca2+=H2O+CaCO3↓ |
下列离子方程式正确的是( )
| A、醋酸溶解鸡蛋壳:2H++CO32-═CO2↑+H2O |
| B、铝片加入烧碱溶液:2A1+2OH-+2H2O═2A1O2-+3H2↑ |
| C、铁与盐酸反应:2Fe+6H+═2Fe3++3H2↑ |
| D、铜片投入FeCl3溶液中:Cu+Fe3+═Cu2++Fe2+ |
下列有关物质的分类或归类正确的是( )
| A、混合物:石炭酸、水玻璃、水银 |
| B、化合物:乙醇、漂白粉、HD |
| C、电解质:明矾、冰醋酸、硫酸钡 |
| D、同系物:CH2O2、C2H4O2、C3H6O2 |
进行中和滴定时,事先不应该用所盛溶液洗涤的仪器是( )
| A、酸式滴定管 | B、碱式滴定管 |
| C、锥形瓶 | D、移液管 |