题目内容
设nA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、标准状况下,22.4L氯气与过量的铁完全反应,转移电子数为2nA |
| B、42gC3H6中含有的共用电子对数目为8nA |
| C、加热下,1molH2和1molI2混合反应生成的气体分子数为2nA |
| D、0.01mol?L-1的KAl(SO4)2溶液中含有0.02nA个SO42- |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、根据氯气反应后的价态来分析;
B、质量换算物质的量结合分子式计算电子数;
C、H2和I2的反应为可逆反应;
D、溶液体积不明确.
B、质量换算物质的量结合分子式计算电子数;
C、H2和I2的反应为可逆反应;
D、溶液体积不明确.
解答:
解:A、氯气反应后的价态为-1价,故1mol氯气参与反应转移2mol电子,故A正确;
B、42g C3H6中物质的量=
=1mol,而1mol丙烯中含9mol共用电子对,故共用电子对数目为9nA,故B错误;
C、H2和I2的反应为可逆反应,故1molH2和1molI2混合后不能反应彻底,所生成的HI分子数小于2nA个,故C错误;
D、溶液体积不明确,无法计算溶液中的硫酸根的个数,故D错误.
故选A.
B、42g C3H6中物质的量=
| 42g |
| 42g/mol |
C、H2和I2的反应为可逆反应,故1molH2和1molI2混合后不能反应彻底,所生成的HI分子数小于2nA个,故C错误;
D、溶液体积不明确,无法计算溶液中的硫酸根的个数,故D错误.
故选A.
点评:本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构、状态是解题关键,难度不大.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、10 mL O.1 mol?L-1NH4C1溶液与5 mL、0.2 mol?L-1NaOH溶液混合:c(Na+)=c(C1-)>c(OH-)>c(NH4+)>c(H+) |
| B、0.1 mol.L-1 pH=4的NaHB的溶液中,c(Na+)>c(HB-) c(H2B)>c(B2-) |
| C、常温时,NaHC03溶液中:c(Na+)=c(HC03-)+c(H2 CO3) |
| D、相同条件下,pH=5的①NH4C1溶液、②CH3COOH溶液、③稀盐酸中由水电离出的c(H+):①>②>③ |
共价键、离子键和分子间作用力是构成物质的微粒间的不同作用方式,下列物质中只存在上述一种作用方式的是( )
| A、二氧化碳 | B、氢氧化钠固体 |
| C、NaCl晶体 | D、氯气 |
NA代表阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,22.4L由氢气和氧气组成的混合气体中,所含有的分子总数为NA |
| B、标准状况下,22.4L氦气中含原子数为2NA |
| C、1mol氯气与足量NaOH溶液反应,转移的电子数为2NA |
| D、1molCH3+(碳正离子)中含有电子数为10 NA |
下列关于金属腐蚀的叙述不正确的是( )
| A、黄铜(铜锌合金)制作的铜锣不易产生铜绿 |
| B、与生铁相比纯铁更容易被腐蚀 |
| C、金属的吸氧腐蚀和析氢腐蚀都属于电化学腐蚀 |
| D、金属腐蚀的本质是M-ne?=Mn+ |
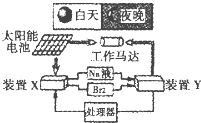 如图是设计的一种航天器能量储存系统原理示意图.它是利用太阳能和物质间的物质变化和能量转换实现循环使用.下列说法正确的是( )
如图是设计的一种航天器能量储存系统原理示意图.它是利用太阳能和物质间的物质变化和能量转换实现循环使用.下列说法正确的是( )| A、二氧化硅是太阳能电池的光电转换材料 |
| B、装置X中阳极反应式:Br2+2e-2Br- |
| C、装置Y中正极反应式为:Br2+2e-2Br- |
| D、有了这套装置后就不用考虑节能减排了 |
运用盖斯定律可方便地计算出难以通过实验直接测定的反应热.已知:
P4(白磷,s)+5O2(g)=P4O10(s)△H=-2983.2kJ?mol-1
P(红磷,s)+
O2(g)=
P4O10(s)△H=-738.5kJ?mol-1
则白磷转化为红磷的热化学方程式为( )
P4(白磷,s)+5O2(g)=P4O10(s)△H=-2983.2kJ?mol-1
P(红磷,s)+
| 5 |
| 4 |
| 1 |
| 4 |
则白磷转化为红磷的热化学方程式为( )
| A、P4(白磷,s)=4P(红磷,s)△H=-29.2kJ?mol-1 |
| B、P4(白磷,s)=4P(红磷,s)△H=+29.2kJ?mol-1 |
| C、P4(白磷,s)=4P(红磷,s)△H=-2244.7kJ?mol-1 |
| D、P4(白磷,s)=4P(红磷,s)△H=+2244.7kJ?mol-1 |
下列有关元素性质比较正确的是( )
| A、碱性:NaOH<Mg(OH)2<Al(OH)3 |
| B、氢化物稳定性:HF>HCl>PH3 |
| C、原子半径:S>F>O |
| D、酸性:HClO>HNO3>H2CO3 |
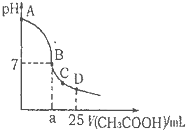 在25mL 0.1mol?L-1 NaOH溶液中逐滴加入0.2mol?L-1 CH3COOH溶液,溶液pH变化曲线如图所示,下列有关离子浓度的比较正确的是( )
在25mL 0.1mol?L-1 NaOH溶液中逐滴加入0.2mol?L-1 CH3COOH溶液,溶液pH变化曲线如图所示,下列有关离子浓度的比较正确的是( )| A、在A、B间任一点(不含A、B点),溶液中可能有c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| B、在C点,c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| C、在B点,a>12.5,且有c(Na+)=c(CH3COO-)>c(OH-)>c(H+) |
| D、在D点,c(CH3COO-)+c(CH3COOH)=c(Na+) |