题目内容
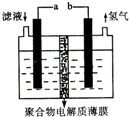 将H2S通人FeCl3溶液中,过滤后将反应液加人电解槽中电解(如图所示)电解后的溶液还可以循环利用.该方法可用于处理石油炼制过程中产生的H2S废气.下列有关说法正确的是( )
将H2S通人FeCl3溶液中,过滤后将反应液加人电解槽中电解(如图所示)电解后的溶液还可以循环利用.该方法可用于处理石油炼制过程中产生的H2S废气.下列有关说法正确的是( )| A、过滤得到的沉淀可能是FeS和S |
| B、若有0.20mol的电子转移,一定能得到2.24L的氢气 |
| C、可以用Fe与外接电源的a极相连 |
| D、与a极相连的电极反应为Fe2+-e-=Fe3+ |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:H2S通人FeCl3溶液,二者之间发生氧化还原反应得到单质硫以氯化亚铁、盐酸的混合溶液,对混合液进行电解,根据电解池的工作原理进行回答即可.
解答:
解:A、H2S通人FeCl3溶液,二者之间发生氧化还原反应得到单质硫的沉淀,没有FeS,故A错误;
B、氯化亚铁、盐酸的混合溶液,在阴极上是氢离子得电子的反应,即2H++2e-=H2↑,有0.20mol的电子转移,得,0.1mol氢气,但是只有在标况下才是2.24L,故B错误;
C、铁为活泼电极,当Fe与外接电源的a极即阳极相连,则金属铁在该电极上失电子,会影响结果,故C错误;
D、在阴极b极上是氢离子得电子的反应,即2H++2e-=H2↑,所以a是阳极,该电极上发生亚铁离子失电子的氧化反应,即Fe2+-e-=Fe3+,故D正确.
故选D.
B、氯化亚铁、盐酸的混合溶液,在阴极上是氢离子得电子的反应,即2H++2e-=H2↑,有0.20mol的电子转移,得,0.1mol氢气,但是只有在标况下才是2.24L,故B错误;
C、铁为活泼电极,当Fe与外接电源的a极即阳极相连,则金属铁在该电极上失电子,会影响结果,故C错误;
D、在阴极b极上是氢离子得电子的反应,即2H++2e-=H2↑,所以a是阳极,该电极上发生亚铁离子失电子的氧化反应,即Fe2+-e-=Fe3+,故D正确.
故选D.
点评:本题考查学生原电池和电解池的工作原理知识,注意氧化还原反应在解题中的作用是关键,难度中等.

练习册系列答案
 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
下列各组离子在指定溶液中,能大量共存的是( )
| A、pH=0溶液:Fe3+、Mg2+、SO42-、NO3- |
B、滴加甲基橙显红色的溶液:Ca2+、K+、MnO4-、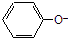 |
| C、1mol?L-1KI溶液中:Cu2+、Fe3+、NO3-、Cl- |
| D、c(NH3?H2O)=1mol?L-1的溶液中:NH4+、Al3+、SO42-、Cl- |
下列关于pH=3的盐酸和醋酸溶液的说法正确的是( )
| A、两种溶液中由水电离出来的c(H+)不相同 |
| B、中和相同体积的两种酸溶液所需NaOH的物质的量分别为a和b,则a<b |
| C、加入足量的铁粉,放出H2的体积相同 |
| D、分别用蒸馏水稀释m倍和n倍,两溶液pH仍相同,则m=n |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、24gO2分子和24gO3分子所含的氧原子数目相等 |
| B、标准状况下,22.4L水中含有的水分子数为NA |
| C、标准状况下,22.4L氯化氢所含的原子数为NA |
| D、1molN2所含有的原子数为NA |
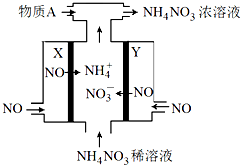 电解NO制备 NH4NO3的工作原理如图所示,X、Y皆Pt电极,为使电解产物全部转化为NH4NO3,需补充物质A.下列说法正确的是
电解NO制备 NH4NO3的工作原理如图所示,X、Y皆Pt电极,为使电解产物全部转化为NH4NO3,需补充物质A.下列说法正确的是( )
| A、物质A为NH3 |
| B、X电极为电解池阳极 |
| C、Y电极上发生了还原反应 |
| D、Y电极反应式为NO-3e-+4OH-═NO3-+2H2O |
用于解释下列现象的化学用语表述正确的是( )
| A、硫化钠溶液呈碱性:S2-+2H2O?H2S+2OH- |
| B、亚硫酸溶液呈酸性:H2SO3═2H++SO32- |
| C、FeCl3溶液呈酸性:Fe3++3H2O?Fe(OH)3+3H+ |
| D、氯化铝溶液跟过量的氨水反应:Al3++4OH-═[Al(OH)4]- |
化学反应伴随能量变化,下列说法中错误的是( )
| A、TNT(炸药)爆炸时部分化学能转化为热能 |
| B、电解饱和食盐水时部分化学能转化为电能 |
| C、镁条燃烧时部分化学能转化为光能 |
| D、植物光合作用时部分光能转化为化学能 |