砹(At)属于卤族元素之一,试推测砹(At)单质及其化合物不可能具有的性质是( )
| A、单质砹易溶于某些有机溶剂 |
| B、AgAt是不溶于水的有色固体 |
| C、HAtO4酸性比HClO4强 |
| D、HAt难溶于水,且受热很难分解 |
密闭容器中,发生反应:CO(g)+2H2(g)?CH3OH(g),△H<0,下列说法正确的是( )
| A、一定温度下,压缩容器体积,则正反应速率加快,逆反应速率减慢 | ||
| B、若甲醇的生成速率等于一氧化碳的消耗速率,则该反应达到平衡状态 | ||
C、升高温度,重新达到平衡时,
| ||
| D、使用催化剂,反应的平衡常数增大 |
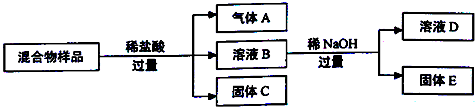
在海水中含有多种元素,开发利用这些资源是科学研究的重要课题.如图为海水利用的部分过程.下列有关说法正确的是( )
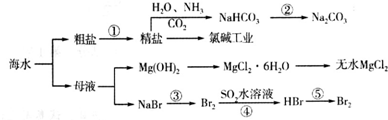

| A、要实现反应②可向NaHCO3溶液中加入过量石灰水 |
| B、溴元素在反应③、⑤中被氧化,在反应④中被还原 |
| C、工业上一般用金属钠与无水MgCl2反应制取Mg单质 |
| D、海水中含有碘元素,可将海水浓缩加热得到碘单质 |
下列各溶液的叙述中不正确的是( )
A、等pH的硫酸与醋酸稀释后pH的变化如图所示,则曲线Ⅱ表示的是醋酸的稀释图象 |
| B、容有等物质的量的NaClO、NaHCO3的溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-) |
| C、若NH4HCO3溶液、NH4HSO4溶液中c(NH4+)相等,则c(NH4HSO4)<c(NH4HCO3) |
| D、已知某温度下Ksp(CH3COOAg)=2.8×10-3,浓度均为0.1mol?L-1的AgNO3溶液和CH3COONa溶液等体积混合一定能产生CH3COOAg沉淀 |
由A、B、C、D四种金属按表中装置进行实验,下列叙述中正确的是( )
| 实验装置与现象 | |||
| 装置 | 甲 | 乙 | 丙 |
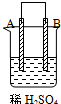 | 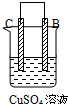 |  | |
| 现象 | A不断溶解 | C的质量增加 | A上有气体产生 |
| A、装置甲中的B金属是原电池的负极 |
| B、装置乙中的C金属是原电池的阳极 |
| C、装置丙中的D金属是原电池的正极 |
| D、四种金属的活泼性顺序是D>A>B>C |
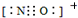
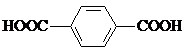 )、4,4′-联吡啶
)、4,4′-联吡啶 (可简化为
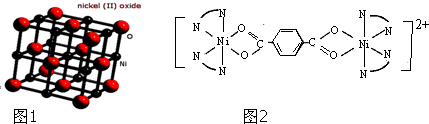
(可简化为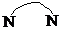 )等与Ni2+能形成多核配合物.配合物[Ni2(TPHA)(bpy)4](ClO4)2络离子的结构如图2:
)等与Ni2+能形成多核配合物.配合物[Ni2(TPHA)(bpy)4](ClO4)2络离子的结构如图2: