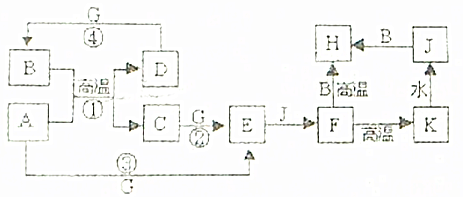
题目内容
将有Mg、Al、Cu组成的粉末状混合物按下图所示进行实验.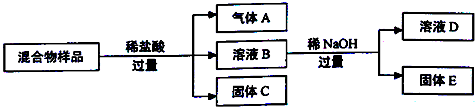
根据实验流程回答下列问题:
(1)气体A的化学式是 .固体E的化学式是
(2)向溶液B中滴加过量NaOH溶液生成溶液D的离子方程式为 .
(3)若在溶液D中逐滴加入盐酸直到过量,则产生的现象是 ,此过程中涉及到的反应的离子方程式为(请写出其中的一条) .
(4)固体C能溶于稀硫酸和H2O2的混合溶液,得到溶液F,由溶液F可以制备胆矾晶体.
①由固体C生成溶液F的化学方程式为 .
②由溶液F制胆矾晶体包含的主要实验操作步骤是:蒸发浓缩、 、洗涤、干燥.

根据实验流程回答下列问题:
(1)气体A的化学式是
(2)向溶液B中滴加过量NaOH溶液生成溶液D的离子方程式为
(3)若在溶液D中逐滴加入盐酸直到过量,则产生的现象是
(4)固体C能溶于稀硫酸和H2O2的混合溶液,得到溶液F,由溶液F可以制备胆矾晶体.
①由固体C生成溶液F的化学方程式为
②由溶液F制胆矾晶体包含的主要实验操作步骤是:蒸发浓缩、
考点:物质分离和提纯的方法和基本操作综合应用,物质分离、提纯的实验方案设计
专题:
分析:由混合物分离流程可知,加过量盐酸得到固体C为Cu,气体A为氢气,溶液B中含镁离子、铝离子及盐酸,再加过量NaOH溶液,固体E为氢氧化镁,溶液D中含偏铝酸钠和NaOH,然后结合元素化合物性质及氧化还原反应来解答.
解答:
解:由混合物分离流程可知,加过量盐酸得到固体C为Cu,气体A为氢气,溶液B中含镁离子、铝离子及盐酸,再加过量NaOH溶液,固体E为氢氧化镁,溶液D中含偏铝酸钠和NaOH,
(1)由上述分析可知,A为H2,E为Mg(OH)2,故答案为:H2;Mg(OH)2;
(2)B中滴加过量NaOH溶液生成溶液D的离子方程式为Al3++4OH?═AlO2-+2H2O (或Al3++3OH?═Al(OH)3↓、Al(OH)3+OH?═AlO2-+2H2O),
故答案为:Al3++4OH?═AlO2-+2H2O (或Al3++3OH?═Al(OH)3↓、Al(OH)3+OH?═AlO2-+2H2O);
(3)溶液D中逐滴加入盐酸直到过量,发生H++OH-═H2O、AlO2-+H++H2O═Al(OH)3↓、Al(OH)3+3H+═Al3++3H2O,则产生的现象是开始无明显现象,后产生白色沉淀,最后沉淀消失,
故答案为:开始无明显现象,后产生白色沉淀,最后沉淀消失;H++OH-═H2O、AlO2-+H++H2O═Al(OH)3↓、Al(OH)3+3H+═Al3++3H2O(任意一个);
(4)①C能溶于稀硫酸和H2O2的混合溶液,得到溶液F,发生氧化还原反应生成F为硫酸铜,化学反应为Cu+H2SO4+H2O2═CuSO4+2H2O,
故答案为:Cu+H2SO4+H2O2═CuSO4+2H2O;
②由CuSO4溶液制胆矾晶体包含的主要实验操作步骤是:蒸发浓缩、冷却结晶、过滤、洗涤、干燥,故答案为:冷却结晶.
(1)由上述分析可知,A为H2,E为Mg(OH)2,故答案为:H2;Mg(OH)2;
(2)B中滴加过量NaOH溶液生成溶液D的离子方程式为Al3++4OH?═AlO2-+2H2O (或Al3++3OH?═Al(OH)3↓、Al(OH)3+OH?═AlO2-+2H2O),
故答案为:Al3++4OH?═AlO2-+2H2O (或Al3++3OH?═Al(OH)3↓、Al(OH)3+OH?═AlO2-+2H2O);
(3)溶液D中逐滴加入盐酸直到过量,发生H++OH-═H2O、AlO2-+H++H2O═Al(OH)3↓、Al(OH)3+3H+═Al3++3H2O,则产生的现象是开始无明显现象,后产生白色沉淀,最后沉淀消失,
故答案为:开始无明显现象,后产生白色沉淀,最后沉淀消失;H++OH-═H2O、AlO2-+H++H2O═Al(OH)3↓、Al(OH)3+3H+═Al3++3H2O(任意一个);
(4)①C能溶于稀硫酸和H2O2的混合溶液,得到溶液F,发生氧化还原反应生成F为硫酸铜,化学反应为Cu+H2SO4+H2O2═CuSO4+2H2O,
故答案为:Cu+H2SO4+H2O2═CuSO4+2H2O;
②由CuSO4溶液制胆矾晶体包含的主要实验操作步骤是:蒸发浓缩、冷却结晶、过滤、洗涤、干燥,故答案为:冷却结晶.
点评:本题考查混合物分离提纯的综合应用,为高频考点,把握金属的性质、流程中的反应及混合物分离方法为解答的关键,注意氢氧化铝的两性及结晶水合物的制备,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列变化,加入还原剂可以实现的是( )
| A、Ag→Ag+ |
| B、Cu→CuO |
| C、Fe2O3→FeO |
| D、NO→NO2 |
表面介导电池(SMCS)是一种新型充电电池,可使电动汽车的充电时间仅需几分钟,该电池的电极材料为金属锂和氧化石墨烯.下列有关说法中不正确的是( )
| A、放电时,氧化石墨烯作正极 |
| B、放电时,负极电极反应式为Li-e-═Li+ |
| C、充电时,该电池是将电能转化为化学能 |
| D、充电时,电解质溶液中的Li+从阴极迁移到阳极 |
设NA为阿伏伽德罗常数的数值,下列说法中正确的是( )
| A、含4 mol Si-O键的二氧化硅晶体中,氧原子数为2NA |
| B、0℃、1个标准大气压下,22.4 L NO 和22.4 L O2混合后,所得气体中的分子总数为1.5NA |
| C、1.8 g重水(D2O)中含有的质子数和电子数均为1.0NA |
| D、将11.2 L Cl2通入足量的石灰乳中制备漂白粉,转移的电子数为0.5NA |
下列物质中,既能跟盐酸反应,又能跟氢氧化钠反应的物质有( )
①Al ②Al2O3 ③Al(OH)3 ④(NH4)2SO4 ⑤Al2(SO4)3 ⑥KHCO3.
①Al ②Al2O3 ③Al(OH)3 ④(NH4)2SO4 ⑤Al2(SO4)3 ⑥KHCO3.
| A、①②③⑤ | B、②③④⑥ |
| C、①②③⑥ | D、①②③④⑥ |
鼠尾草酚可用于防治骨质疏松,鼠尾草酸可两步转化得到鼠尾草酚,下列说法正确的是( )

| A、X、Y、Z分子中均含有2个手性碳原子 |
| B、X、Y、Z均能与FeCl3溶液发生显色反应 |
| C、1mol Y最多能消耗2molH2 |
| D、1molZ与NaOH溶液反应最多消耗3molNaOH |