题目内容
硼、镁及其化合物在工农业生产中应用广泛.
已知:硼镁矿主要成分为Mg2B2O5?H2O,硼砂的化学式为Na2B4O7?10H2O.利用硼镁矿制取金属镁及粗硼的工艺流程为:

回答下列有关问题:
(1)硼砂溶于热水后,常用H2SO4调pH2~3制取H3BO3,反应的离子方程式为 .
H3BO3微溶于水,为一元弱酸,但其酸性并不是源于其结构中羟基的电离,请写出其电离方程式 .
(2)MgCl2?7H2O需要在HCl氛围中加热,其目的是 .若用惰性电极电解MgCl2溶液,其阴极反应式为 .
(3)镁-H2O2酸性燃料电池的反应机理为Mg+H2O2+2H+═Mg2++2H2O,则正极反应式为 .若起始电解质溶液pH=1,则pH=2时溶液中Mg2+离子浓度为 .已知Ksp[Mg(OH)2]=5.6×10-12,当溶液pH=7时 (填“有”或“没有”)Mg(OH)2沉淀析出.
(4)制得的粗硼在一定条件下生成BI3,BI3加热分解可以得到纯净的单质硼.现将 0.020g粗硼制成的BI3完全分解,生成的I2用0.30mol?L-1 Na2S2O3(H2S2O3为弱酸)溶液滴定至终点,消耗Na2S2O3溶液18.00mL.盛装Na2S2O3溶液的仪器应为 滴定管(填“酸式”或“碱式”).该粗硼样品的纯度为 .(提示:I2+2S2O32-=2I-+S4O62-)
已知:硼镁矿主要成分为Mg2B2O5?H2O,硼砂的化学式为Na2B4O7?10H2O.利用硼镁矿制取金属镁及粗硼的工艺流程为:

回答下列有关问题:
(1)硼砂溶于热水后,常用H2SO4调pH2~3制取H3BO3,反应的离子方程式为
H3BO3微溶于水,为一元弱酸,但其酸性并不是源于其结构中羟基的电离,请写出其电离方程式
(2)MgCl2?7H2O需要在HCl氛围中加热,其目的是
(3)镁-H2O2酸性燃料电池的反应机理为Mg+H2O2+2H+═Mg2++2H2O,则正极反应式为
(4)制得的粗硼在一定条件下生成BI3,BI3加热分解可以得到纯净的单质硼.现将 0.020g粗硼制成的BI3完全分解,生成的I2用0.30mol?L-1 Na2S2O3(H2S2O3为弱酸)溶液滴定至终点,消耗Na2S2O3溶液18.00mL.盛装Na2S2O3溶液的仪器应为
考点:物质分离和提纯的方法和基本操作综合应用,探究物质的组成或测量物质的含量
专题:实验设计题
分析:硼镁矿主要成分为Mg2B2O5?H2O,硼砂的化学式为Na2B4O7?10H2O.利用硼镁矿制取金属镁及粗硼的工艺流程中硼镁矿加入氢氧化钠浓溶液过滤,滤渣中加入浓盐酸得到氯化镁,加入浓盐酸溶解通过蒸发浓缩得到氯化镁结晶水合物,在氯化氢气流中加热得到氯化镁固体,电解得到镁;滤液中主要是NaBO2,通入适量二氧化碳气体得到硼砂,溶于热水后,用H2SO4调pH2~3制取H3BO3,加热得到X为B2O3,
(1)硼砂的化学式为Na2B4O7?10H2O,用H2SO4调pH2~3,硼砂中的Na2B4O7在酸溶液中生成H3BO3 ,H3BO3微溶于水,为一元弱酸,但其酸性并不是源于其结构中羟基的电离,应结合水电离生成OH-,促进水的电离;
(2)氯化镁在水溶液中水解生成氢氧化镁,加入盐酸可抑制水解;惰性电极电解MgCl2溶液阴极氢离子得到电子生成氢气,水的电离平衡破坏,水电离生成氢氧根离子浓度增大,和镁离子形成氢氧化镁沉淀,合并写出电极反应;
(3)燃料电池中正极上是过氧化氢得到电子生成水;依据电解质溶液PH变化结合电池反应计算镁离子浓度;PH=7计算氢氧根离子浓度,结合生成镁离子浓度计算浓度商和溶度积常数比较分析是否生成氢氧化镁沉淀;
(4)根据关系式B~BI3~
I2~3S2O32-及滴定数据计算出粗硼中硼的含量.
(1)硼砂的化学式为Na2B4O7?10H2O,用H2SO4调pH2~3,硼砂中的Na2B4O7在酸溶液中生成H3BO3 ,H3BO3微溶于水,为一元弱酸,但其酸性并不是源于其结构中羟基的电离,应结合水电离生成OH-,促进水的电离;
(2)氯化镁在水溶液中水解生成氢氧化镁,加入盐酸可抑制水解;惰性电极电解MgCl2溶液阴极氢离子得到电子生成氢气,水的电离平衡破坏,水电离生成氢氧根离子浓度增大,和镁离子形成氢氧化镁沉淀,合并写出电极反应;
(3)燃料电池中正极上是过氧化氢得到电子生成水;依据电解质溶液PH变化结合电池反应计算镁离子浓度;PH=7计算氢氧根离子浓度,结合生成镁离子浓度计算浓度商和溶度积常数比较分析是否生成氢氧化镁沉淀;
(4)根据关系式B~BI3~
| 3 |
| 2 |
解答:
解:(1)硼砂的化学式为Na2B4O7?10H2O,用H2SO4调pH2~3,硼砂中的Na2B4O7在酸溶液中生成H3BO3 ,反应的离子方程式为:B4O72-+2H++5H2O=4H3BO3,
H3BO3微溶于水,为一元弱酸,但其酸性并不是源于其结构中羟基的电离,应结合水电离生成OH-,促进水的电离,其电离方程式为H3BO3+H2O?B(OH)4-+H+,
故答案为:B4O72-+2H++5H2O=4H3BO3;H3BO3+H2O?B(OH)4-+H+;
(2)MgCl2?7H2O需要在HCl氛围中加热,是为了防止氯化镁水解生成氢氧化镁;若用惰性电极电解MgCl2溶液,阴极氢离子得到电子生成氢气,水的电离平衡破坏,水电离生成氢氧根离子浓度增大,和镁离子形成氢氧化镁沉淀,合并写出阴极反应式为:2H2O+Mg2++2e-=H2↑+Mg(OH)2↓;
故答案为:防止MgCl2水解生成Mg(OH)2;2H2O+Mg2++2e-=H2↑+Mg(OH)2↓;
(3)镁-H2O2酸性燃料电池的反应机理为Mg+H2O2+2H+═Mg2++2H2O,正极上是过氧化氢得到电子生成水的反应,正极反应式H2O2+2H++2e-=2H2O;
若起始电解质溶液pH=1,则pH=2时溶液中,氢离子浓度减小0.1mol/L-0.01mol/L=0.09mol/L,依据反应方程式得到c(Mg2+)=
c(H+)减小=0.045mol/L;
Ksp[Mg(OH)2]=5.6×10-12,当溶液pH=7时,c(OH-)=10-7mol/L,则Qc=c(Mg2+)×c2(OH-)=0.045mol/L×10-14mol/L=4.5×10-16<Ksp[Mg(OH)2],说明无氢氧化镁沉淀生成;
故答案为:H2O2+2H++2e-=2H2O;0.045 mol?L-1;没有;
(4)Na2S2O3溶液呈碱性,应放在碱式滴定管中,
硫代硫酸钠的物质的量为:0.30mol/L×0.018L=0.0054mol,
根据关系式:B~BI3~
I2~3S2O32-,
n(B)=
n(S2O32-)=0.0018mol,
硼的质量为:10.81g/mol×0.0018mol=0.01944g,粗硼中硼的含量为:
×100%=97.2%,
故答案为:碱式;97.2%.
H3BO3微溶于水,为一元弱酸,但其酸性并不是源于其结构中羟基的电离,应结合水电离生成OH-,促进水的电离,其电离方程式为H3BO3+H2O?B(OH)4-+H+,
故答案为:B4O72-+2H++5H2O=4H3BO3;H3BO3+H2O?B(OH)4-+H+;
(2)MgCl2?7H2O需要在HCl氛围中加热,是为了防止氯化镁水解生成氢氧化镁;若用惰性电极电解MgCl2溶液,阴极氢离子得到电子生成氢气,水的电离平衡破坏,水电离生成氢氧根离子浓度增大,和镁离子形成氢氧化镁沉淀,合并写出阴极反应式为:2H2O+Mg2++2e-=H2↑+Mg(OH)2↓;
故答案为:防止MgCl2水解生成Mg(OH)2;2H2O+Mg2++2e-=H2↑+Mg(OH)2↓;
(3)镁-H2O2酸性燃料电池的反应机理为Mg+H2O2+2H+═Mg2++2H2O,正极上是过氧化氢得到电子生成水的反应,正极反应式H2O2+2H++2e-=2H2O;
若起始电解质溶液pH=1,则pH=2时溶液中,氢离子浓度减小0.1mol/L-0.01mol/L=0.09mol/L,依据反应方程式得到c(Mg2+)=
| 1 |
| 2 |
Ksp[Mg(OH)2]=5.6×10-12,当溶液pH=7时,c(OH-)=10-7mol/L,则Qc=c(Mg2+)×c2(OH-)=0.045mol/L×10-14mol/L=4.5×10-16<Ksp[Mg(OH)2],说明无氢氧化镁沉淀生成;
故答案为:H2O2+2H++2e-=2H2O;0.045 mol?L-1;没有;
(4)Na2S2O3溶液呈碱性,应放在碱式滴定管中,
硫代硫酸钠的物质的量为:0.30mol/L×0.018L=0.0054mol,
根据关系式:B~BI3~
| 3 |
| 2 |
n(B)=
| 1 |
| 3 |
硼的质量为:10.81g/mol×0.0018mol=0.01944g,粗硼中硼的含量为:
| 0.01944g |
| 0.0200g |
故答案为:碱式;97.2%.
点评:本题综合考查物质的分离、提纯以及制备,为高考常见题型,侧重于学生的分析、实验和计算能力的考查,题目涉及盐类的水解、原电池原理和电解池原理的分析,沉淀溶解平衡的计算应用,题目难度稍大,计算是难点,计算时要充分利用题目所给数量关系和表中数据,根据质量关系和质量分数的概念快速解题.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
下列各组离子能大量共存于同一溶液中的是( )
| A、Ba2+、Mg2+、Cl-、CO32- |
| B、Fe3+、K+、I-、SO42- |
| C、K+、NH4+、NO3-、OH- |
| D、Al3+、NH4+、NO3-、Cl- |
通常状况下,下列物质为气体的是( )
| A、甲苯 | B、溴乙烷 |
| C、四氯化碳 | D、2-甲基丙烷 |
 氧化还原是常见的反应类型,根据信息回答以下问题:
氧化还原是常见的反应类型,根据信息回答以下问题: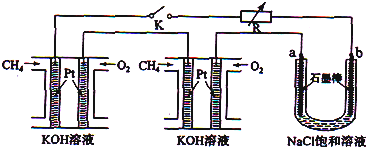

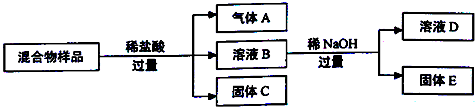
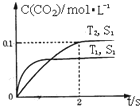 2013年雾霾天气多次肆虐我国中东部地区.其中,汽车尾气和燃煤尾气是造成空气污染的原因之一.
2013年雾霾天气多次肆虐我国中东部地区.其中,汽车尾气和燃煤尾气是造成空气污染的原因之一.